根据ctDNA量化的肿瘤突变负荷可很好的预测转移性NSCLC患者是否能从免疫治疗中获益
肿瘤突变负荷(TMB)已被证明可预测接受免疫检查点抑制剂治疗的非小细胞肺癌(NSCLC)患者的生存获益。采用循环游离肿瘤DNA (ctDNA)检测血液中的TMB (bTMB)比检测组织中的TMB (tTMB)具有实际的优势;然而,仍需要验证试验和鉴别最佳阈值。本文报道了一种新的bTMB算法的分析验证及临床应用。
肿瘤突变负荷(TMB)已被证明可预测接受免疫检查点抑制剂治疗的非小细胞肺癌(NSCLC)患者的生存获益。采用循环游离肿瘤DNA (ctDNA)检测血液中的TMB (bTMB)比检测组织中的TMB (tTMB)具有实际的优势;然而,仍需要验证试验和鉴别最佳阈值。本文报道了一种新的bTMB算法的分析验证及临床应用。
进行临床验证的数据集来源于III期MYSTIC试验,该试验评估了采用durvalumab(抗PD-L1抗体)± tremelimumab(抗细胞毒性T淋巴细胞相关抗原4抗体)或化疗作为一线疗法治疗转移性NSCLC。同时评估了患者的bTMB(GuardantOMNI实验)和tTMB(FoundationOne CDx实验)。
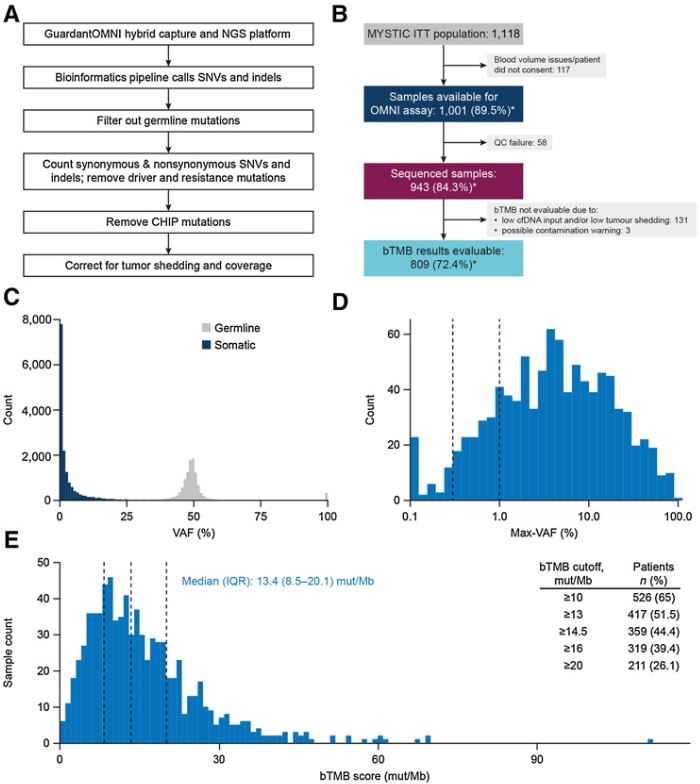
研究流程和患者的bTMB评分
在MYSTIC试验中,在大部分患者的血浆样本抽提出的ctDNA中可检测到体细胞突变,随后可计算bTMB。bTMB组的有效TMB得分成功率高于tTMB组(81% vs 63%)。验证分析的最新P值证实,bTMB≥20 个突变/兆碱基(mut/Mb)可选作为从durvalumab+tremelimumab联合治疗中获益的最适阈值。
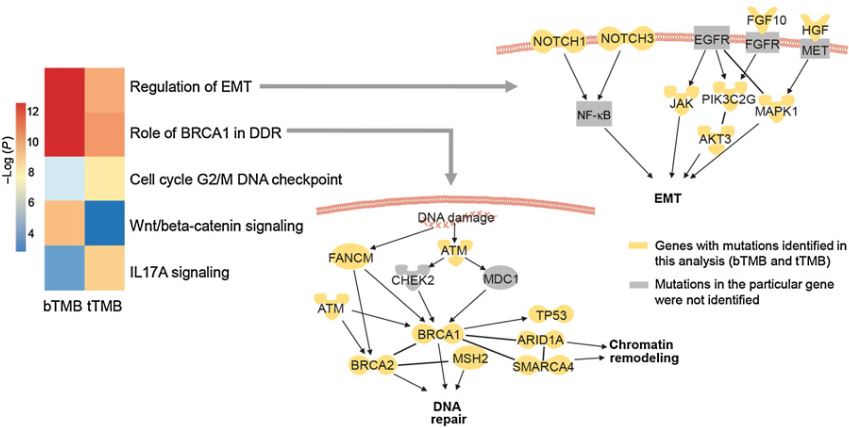
高TMB患者(bTMB≥20 mut/Mb或tTMB≥10 mut/Mb)的突变富集通路
总之,该研究展现了以GuardantOMNI ctDNA平台量化血浆bTMB的可行性、准确性和可重复性。采用新的bTMB算法和最佳bTMB阈值(≥20 mut/Mb),高bTMB是转移性NSCLC患者从durvalumab+tremelimumab或化疗中获益的预测指标。
原始出处:
Han Si, et al.Blood-based Assay for Assessment of Tumor Mutational Burden in First-line Metastatic NSCLC Treatment: Results from the MYSTIC Study. Clin Cancer Res February 1 2021 DOI:10.1158/1078-0432.CCR-20-3771