PLOS computational biology:AI融合基因组学研究预测阿尔茨海默病的早期分子标记
PLOS computational biology:AI融合基因组学研究预测阿尔茨海默病的早期分子标记
导言:下一代测序(NGS)技术已经成为剖析各种人类疾病的分子和病理特征的强大工具,然而,来自不同疾病阶段的生物样品的有限性是研究疾病进展和识别早期病理变化的主要障碍。近期,韩国脑科学研究所的研究人员使用了一种深度学习技术,利用人工智能(AI)融合基因组学研究预测阿尔茨海默氏病(AD)的早期分子标记。
近年来,深度学习技术不断推动着人工智能(AI)技术革命。受下一代测序(NGS)技术进步的启发,基于组学的研究数据已经变得易于访问和标准化。近日,韩国脑科学研究所的一项研究使用先进的对抗性生成网络(GANs)的深度学习技术分析了阿尔茨海默氏病(AD)小鼠模型的大脑皮质组织数据。结果发现,β淀粉样蛋白在疾病的早期含量增加并改变胆固醇的生物合成。
该研究发表在计算生物学领域的国际学术期刊《PLOS计算生物学》上。题为“A practical application of generative adversarial networks for RNA-seq analysis to predict the molecular progress of Alzheimer's disease”

β淀粉样蛋白是导致阿尔茨海默氏病(AD)的一种蛋白质。在正常的大脑中,如果过度积累,则会被小胶质细胞等清除。胆固醇也必须在血液中保持一定水平,以组成细胞膜,调节膜的流动性并保持体内平衡。如果上述过程不能正常进行,则体内会发生病理异常。
研究团队使用先进的对抗性生成网络(GANs)的深度学习技术分析了AD小鼠模型的大脑皮质组织数据。GANs是一种算法,它通过生成器和鉴别器之间的竞争来生成数据,分析生成的数据,并生成接近真实图像的合成数据。先前,GANs技术曾用于制作巴拉克·奥巴马(Barack Obama)总统的假演讲视频,并可用于预测面部老化。
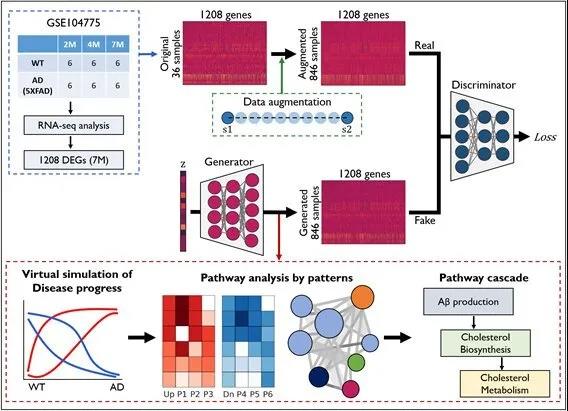
GAN在大量RNA-seq数据中的应用概述。图片来源:韩国脑科学研究所
研究小组利用GANs对小鼠进行了AD基因表达模拟,观察了基因表达从正常状态到AD状态的变化过程。结果发现β淀粉样蛋白在疾病早期含量增加并改变了胆固醇的生物合成。这一发现也被死后脑组织的RNA序列分析所证实。
这意味着β淀粉样蛋白的增加会触发胆固醇的生物合成,这两个过程结合在一起很可能通过相互作用影响突触形成和突触可塑性。
这项研究是基于生物信息学与AI融合的独特研究技术,其意义在于为研究者提供更系统的分析和实验设计,它代表了一种新的方法来预测疾病发展早期阶段的生物变化,并可以将其应用于医疗保健行业。
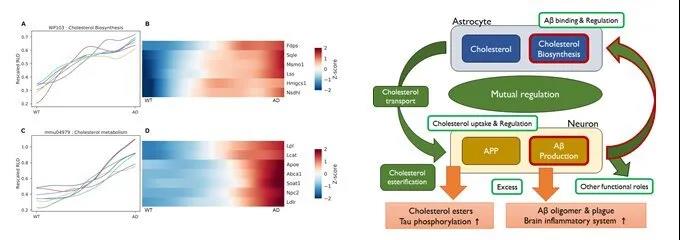
与胆固醇生物合成和胆固醇代谢有关的基因的过渡曲线和热图。图片来源:韩国脑科学研究所
Cheon博士表示:“ GANs是一个有用的工具,可以用来分析由疾病引起的基因表达差异,并通过解释现象的原因来分析其分子进展。这种方法的不断扩展和组学数据的积累有望帮助我们克服与脑疾病和衰老相关的分析的最大局限性,这是一个耗时的获取样本的过程。”
这项研究是由KBRI独家资助的项目。
原始出处:
Jinhee Park, Hyerin Kim, Jaekwang Kim, et.al.A practical application of generative adversarial networks for RNA-seq analysis to predict the molecular progress of Alzheimer's disease.PLOS COMPUTATIONAL BIOLOGY July 24, 2020






