失血性休克的该管理:生理学方法、时机和策略!
摘要 失血性休克(Hemorrhagic shock,HS)的管理是基于及时、快速、确定性出血源头的控制和失血量的补充。阻断所有可见血管的活动性出血是有效的而且也是最主要的最基本的临床原则,同时也是最重要的、必须的、挽救生命的步骤。输血目的是预防缺血/再灌注毒血症,优化组织氧合和微循环。失血性休克的生理学分期决定了及时的处理,它适于损伤控制外科(DCS)的战略和滴定式低血压复苏(THR)的战术。
摘要
失血性休克(Hemorrhagic shock,HS)的管理是基于及时、快速、确定性出血源头的控制和失血量的补充。阻断所有可见血管的活动性出血是有效的而且也是最主要的最基本的临床原则,同时也是最重要的、必须的、挽救生命的步骤。输血目的是预防缺血/再灌注毒血症,优化组织氧合和微循环。失血性休克的“生理学分期”决定了及时的处理,它适于“损伤控制外科(DCS)”的战略和“滴定式低血压复苏(THR)”的战术。在任何出现了低血压但尚未达到危急的休克中,机体对液体负荷测试的反应性决定了是采取保守治疗和准备手术,还是送到手术室进行快速控制出血源头之间的代偿和进展之间的分界点。用于补充非张力的静脉回流容量最高可达总血容量的20%。在任何危急程度的休克中,患者从一开始就表现出临界生理和即将发生的心脏骤停或心血管事件的迹象,到求生反射延伸到最大程度,比如远端灌注不足(血液、氧气和代谢底物)之间的平衡保持在脆弱和微妙的平衡状态,这时很容易受到任何微小变化或干预因素的影响。在放血引起的心脏骤停的动物的研究中,生理问题的核心仍然是快速恢复充足的静脉回流,允许通过正中开胸或前外侧开胸进行开放式心脏按摩,或在体外复苏和诱导低温下在胸腔或腹部夹住主动脉后自发地将静脉回流到全身循环中。这是预防心脑缺血性损伤的唯一方法。而且这只能通过直接入路快速有效地完成,如果出血来自腹部+/−下肢部位,则采用挤压剖腹手术,如果出血来自胸部+/−上肢部位,则采用快速胸骨切开/胸前外侧切开。如果不先止血,不给心脏恢复血容量,那么任何进一步的努力都注定失败。通过剖腹/开胸手术直接控制血源头,同时进行或紧接着进行静脉再灌注,这是两个最基本的、最早的挽救生命的步骤。
1. 介绍
自2010年以来,出血性休克的“生理学分期”已被提出,其概念基于休克的正确定义、身体的天然止血机制、微循环/小动脉系统的新进展、“心脏/循环储备”的概念以及基本的生理学考量,如流体-阻力性低血压的重要性。这是一种临床分期,非常适合管理和实施损伤控制手术(Damage control surgery, DCS)和滴定式低血压复苏(Titrated hypotensive resuscitation, THR)的最佳时机 (图1和2)。与此相关的是,它给既往混乱的文献带来了一些规则,出现了一些新的名词,如死亡三联症和损伤控制复苏,但这些都没有产生实际的益处。


目前,只有通过经胸超声心动图(TTE)进行体内外周微循环可视化和连续心排量(CO)监测,才能增加预测休克代偿或失代偿程度的临床评估。同时联合组织缺氧的评估,如中心静脉血氧饱和度(ScvO2),将是受欢迎的。
人工智能可以帮助预测休克代偿、代偿的能力和代偿持续的时间。但在人工智能测量其大循环和微循环的实时休克动力学方面变得更加精细和复杂之前,对休克的管理和干预的时机仍是基于患者当前血液动力学紊乱程度和与之相关的体征的临床评估。
迄今为止,这项研究仍在进行中。连续、实时的动脉波形分析(AWFA)可以在正常生命体征变化之前提供早期出血的预警和显性休克发作的提示,并能够早期区分“差的”代偿(即,对失血的耐受性相对降低)和“好的”代偿(即,对失血的耐受性相对较好)。最近,共振拉曼光谱技术(Raman spectroscopy)在组织氧合测量方面取得了进展,该技术似乎与标准的传统方法(如 ScvO2)一样快速准确。目前还没有方法能够足够容易和准确地实时测量心脏/循环储备和组织氧合,以进行完美的及时决策。
1.1. 心脏储备和液体负荷试验
无论是心源性休克、脓毒性休克还是失血性休克,任何危急情况都不能忽视三个基本的生理学概念:液体反应性、心脏/循环储备、微循环,尤其是远端组织灌注所依赖的小动脉系统。
心脏储备,在失血性休克的情况下更好地用术语“循环储备”来定义,是在运动过程中或为了补偿生理极限内的不足,心脏可以泵入高于基线水平的最大血液量。心肌功能储备越差或变得越低,则心泵失效后休克发生的可能性就越大,这是根据Frank-Starling定律,健康部分的心肌能够在舒张期对静脉回流变化作出反应,同时收缩性增加。这是因为顺应性降低导致左/右心室舒张末期压力增加,导致室壁张力增加和耗氧量(VO2)增加,进而降低心输出量。正如Convertino所说,任何生理性代偿机制(如心动过速和血管收缩)对任何特定应激(如出血)都有一个最大反应的天花板效应。“储备”代偿也可以定义为最大反应和基线状态之间的差值。
通常利用休克的临床观察,收缩压(SBP)通常作为心输出量(CO)的直接反映,并将其与一般临床情况相关联。
老年人,如果没有心肌或瓣膜疾病或心律失常或高血压,尤其同时存在脑创伤(TBI)或干扰药物(比如β-blocker),则循环/心脏储备正常的患者,SBP对液体负荷的反应可以作为CO的粗略指导。如果在液体负荷试验20-30分钟后,SBP及其非直接相关的心动过速没有改善且依然保持原样,则可以认为当前的心脏/循环储备及其直接相关的CO不足以保持患者血液动力学稳定。
对SBP正常化和心动过速逆转趋势有反应的患者被视为“反应者”。
如果CO及其直接变量——收缩压和心动过速——在20分钟的观察期内没有改善且保持原样,则可以认为目前的机体储备能力不足以保持患者血液动力学稳定。这种情况定义为 “无反应者”。
由于与静脉回流的直接关系,对液体负荷的CO直接系列反应将是我们可以用来测量心脏/循环储备的最可靠的参数。
液体负荷试验(可以多次)后5-10分钟内,可在床旁用经胸超声心动图(TTE)直接连续测量CO。患者应接受至少20分钟的重复常的规超声心动图监测,在肾功能衰竭的情况下可达30分钟,以排除一过性的反应
超声心动图测得的CO总是先于心动过速和血压的变化。
超声心动图需要技能和经验才能非常准确,但仍然是直接快速监测CO的最佳方法。
静脉回流压力梯度的变化,定义为液体挑战后体循环平均充盈压(Pmsf)和中心静脉压(CVP)之间的差异,在对液体有反应者中可观察到,但在无反应者中看不到。在无反应者中,体循环平均充盈压的增加仅转化为CVP的增加(不能转化为CO的增加)。在那些有反应的受试者中,CO的最大变化出现在液体挑战完成后的1分钟。
体循环平均充盈压是在血管中血液没有流动时(如在循环停止时)对血管壁压力的测量值。参照血管壁张力,血管内容积被很好地分为“张力容积”和“非张力容积”。非张力性容积充满容器,但不产生任何张力。张力性容积可导致容器壁的拉伸,并增加容器内的张力。如果液体挑战是有效的,那么它将会增加张力体积,至少可表现为一过性的,并导致体循环平均充盈压上升。这样就增加了心脏的前负荷,根据Frank-Starling原理,最终增加了有前负荷反应性患者的CO。
如果给予液负荷测试,能有效地显著增加体循环平均充盈压,但没有观察到随后的CO增加,则患者被定义为无反应者。在正常血容量条件下,例如在脓毒性休克中,如果患者对液体有反应,即具有功能性小动脉系统,有效的液体挑战将导致每搏输出量显著增加10%以上,或者与20分钟内重复检查的结果是一致的。
CO的增加是一种短暂的反应:输液10分钟后,CO恢复到基线值。脓毒性休克中液体负荷试验的最佳量为≥4 mL/kg,这也是失血性休克中用于低血压复苏的重复剂量中附带使用的量。在炎性或分布性休克和失血性休克中的液体挑战有实质性的不同,前者的正常血容量,后者的血容量减少。
尽管脓毒性休克(液体挑战试验已被广泛研究)和失血性休克(就血容量而言)之间的动力学之间存在差异,但其基本原理是一样的,经过适当的修改,可以应用于失血性休克的管理并可靠地标准化。
在急性低血容量状态中,如在表现为低血压的失血性休克中,应给予足够量的液体负荷试验,以首先使容量/压力(V/P)比值达到低于低血压发生时更低的水平,同时,保持该比值不接近1,以防止抵消生理性止血机制。
由于在脓毒性休克的情况下不存在低血容量,只有首先增加平均全身充盈压(Pmsf ),才有可能清楚在失血性休克的评估中是否可以依赖液体挑战试验。在进行性低血压休克中,液体挑战的目的是确定失血是否已经由生理机制和功能性小动脉系统控制,或者正在进行,我们正在处理未控制的出血。
因此,恢复导致低血压的血容量损失是第一步,成人的血容量损失至少为TBV的20%(此时会出现失血性休克失代偿)。
在成人中超过这个量时,例如,1.5 L,其等于大约30%的TBV,并且如果该血容量丢失到达会导致持续低血压的量时,实际上可能会通过抵消生理止血机制而增加出血。
因此,执行以下步骤顺序可以被视为一种合理且可接受的策略。如果没有观察到血流动力学变化,尤其是SBP正常化和心动过速的逆转趋势,则在5分钟内给予500ml的大剂量液体,并在接下来的5-10分钟内再次重复。观察对CO或血压可能有意义的影响。再等10-20分钟,看看SBP的增加是否保持稳定。
这一经验性剂量已被正常血容量的脓毒性休克的经验和一项研究间接证实,在该研究中,一组钝性外伤但无院前低血压的患者接受 > 500 mL大剂量prn后,与一组院前低血压患者接受相同大剂量相比,死亡率增加。追加量恰好是7mL/kg和10%的TBV。
在此阶段,补液试验主要是支持大循环;如果还能促进微循环血流动力学,则效果更好。
高渗盐水(HTS)可能是失血性休克合并脑创伤患者的最佳液体种类,但不能超过375 mL/h。如果使用HTS,应在使用另一种液体之后,因为一种液体的剂量不能超过250 mL/h (1.5 h内最多375 mL),以最大限度地发挥其优点,减少其对出血影响的缺点,因为它通过干扰凝血和可能诱导的压力升高作为直接的血流动力学效应。
实际上,任何胶体液或晶体液都可以用作液体负荷试验的选择。
在失血性休克临床II期和III期之间的这个阶段,宝贵的血浆和成份血液应该被保留在后面使用。
1.2.代偿性的稳定性休克的管理方案
一旦液体负荷试验确定小动脉系统功能正常,中等休克水平对晶体和PRBC(浓缩红细胞) 输注反应良好。常规的凝血试验(CCT)可用于凝血筛查。在代偿性休克中不需要进行常规粘弹性止血测试(VHA)。出血源头控制后应立即进行输血,直到血红蛋白水平令人满意为止。健康患者Hb≥7 g/dL,Hct≥22%;心脏病患者Hb≥9 g/dL,Hct≥27%。SvO2最低水平为70%,NBE < 4 meq/L, Lac < 4 mmol/L且无感染是可接受的终点。
患者不需要立即或快速手术,但可以在术前进行CT扫描或影像学检查,并考虑保守治疗。管理原则保持不变:出血源头控制越早,结果越好,特别是对于不可避免的缺血-再灌注毒血症(该毒血症总是潜在的并与缺血的持续时间和程度成比例)。
在代偿稳定的患者中,在出血源头控制之前,最长时间超过4-6小时是安全的,从乡村外科或卫生系统处于发展中的国家或战争场景的经验来看,即使6小时之内缺乏治疗,代称性失血性休克也有很大的存活概率。
这些观察结果对于采用非手术治疗(non- surgery -management, NOM)治疗非主动出血患者的创伤至关重要,出血患者可通过实质组织或器官的解剖边界(如肝脏)进行包埋组织出血。6小时的极限是创伤后炎症反应完全爆发所需的时间。这个极限也是触诊引发腹部出血的炎症反应的最安全的时间。
情况稳定的穿透伤患者可承受干预延迟达2小时而无并发症。
非手术治疗的决定取决于患者的一般情况,血流动力学稳定,无腹部压痛,当前无出血,并在解剖边界上确定有出血源头。
6-8小时后血流动力学稳定且到达手术机构的患者,如果没有与重要结构相邻的异物或腹膜炎,可以进行非手术治疗。患者的监测取决于受伤部位的类型,从2天到7-10天不等。
只有检查条件许可时(无低血压、轻-中度代偿性失血性休克),并且其检查目的仅仅为了确定出血的来源和术前伴随的病理情况。
在伴有外伤性创伤的老年高血压患者中,血压在正常范围内的任何下降都应被视为低血压,比如,收缩压在110-120 mmHg应被视为休克。
休克指数在创伤的情况下可能不太可靠,因为疼痛、炎症反应、低氧血症或高碳酸血症可使心率增快,但它在非创伤性出血中是一个有用的指标。
2. 低血压、不稳定、失代偿、进展性休克III期
如果对液体负荷试验无反应或只有短暂反应(<20-30 min),即快速血流动力学补偿反射完全达到饱和状态时,患者可被视为处于不稳定的晚期休克,小动脉阻力系统的衰竭或功能障碍代偿失调,并伴有出血进展。如果出现对液体负荷无反应的渐进性休克,则不应进行进一步检查。
随后的处理取决于所面对的出血是发生在院前还是院内,以及是动脉、静脉出血还是混合性/未知的出血(图3)
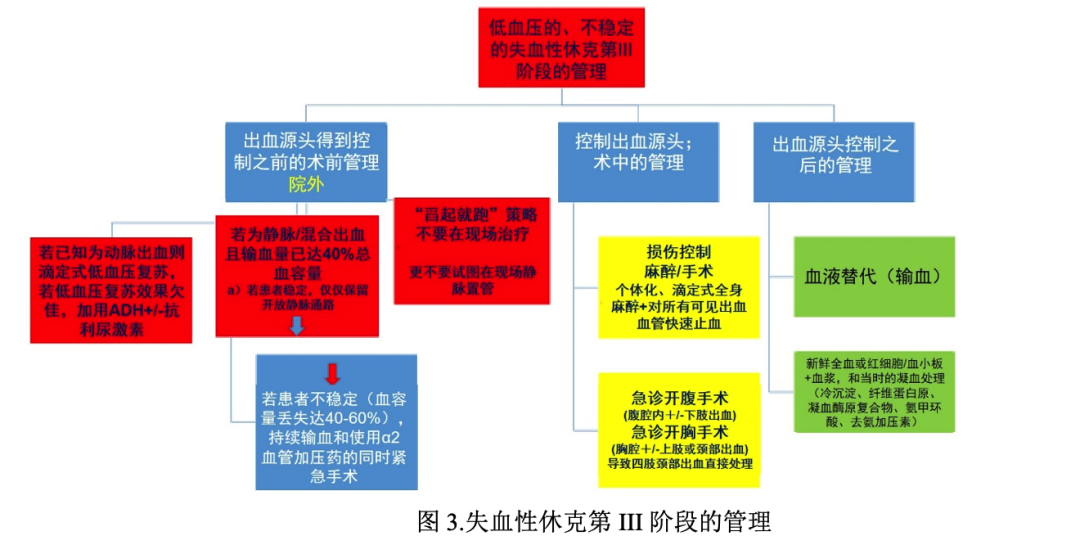
2.1.院外管理
2.1.1.滴定式低血压复苏
如果已知或极有可能出血来源于动脉,应采用“滴定式低血压复苏”(THR)策略。
THR的策略是从低血压对自发减少或停止出血的有益作用的历史观察中发展而来的。在出血源头得到控制之前,正常压力不利于抵消止血的生理机制(动脉出血时的低血压、动脉痉挛和血管收缩,静脉出血时的凝块形成)。
HR(低血压复苏)不适用于15-16岁以下的儿童、高血压老年人(正常范围内的任何血压下降都应被视为单纯的低血压),以及孕妇(任何低血压都表明TBV损失> 35%,是危及生命的不祥之兆)。
确定性出血的静脉来源是低血压复苏的另一个禁忌症。
该策略的目的是将患者的意识水平和平均灌注压保持在足够的水平,以降低缺血再灌注毒血症(IRT)的影响,并防止动脉出血中静脉回流不足导致的心脏骤停性死亡。
根据它的定义,滴定式复苏只能在动脉出血的情况下起作用。如果应用于静脉或常见的静脉出血,滴定式复苏实际上会加速生理恶化,因为它减少了填充完整静脉系统所有部分可能需要的液体量,减少了回心血量,并加速失血。
如果低血压复苏没有达到在不稳定患者中保持最小安全平均动脉压(MAP)的目标,那么该患者正在升级到失血并进入IV期或即将发生心脏骤停的临界失血性休克水平。
正是在短期稳定后持续反复不稳定的暂时性液体反应子群中,以及在已知的动脉或假定的此类出血中,THR找到了其最佳和最有用的应用,旨在赶往最近的外科设施进行挤压GA/外科手术时保持意识水平和最低限度足够的MAP
低血压复苏没有明确显示对发病率和死亡率有益的原因是缺乏统一的荟萃分析,包括适应症、生理紊乱、出血的起源和医源性血管收缩支持的时机。
如果没有正确的病理生理学解释、动态生理学分期和对患者的实时解读,低血压复苏可能会变成一个破坏性的噱头
2.1.2. 低血压复苏策略应该使用多少液体?
在民用和军用环境中的临床经验表明,250 mL大剂量液体,无论是不同浓度的晶体、胶体或高渗盐水(HTS ),作为失血性休克患者有效和安全的初始治疗,都是有益和安全的。
这个液体量大约相当于TBV的5%。如果使用HTS,应接着使用另一种液体,因为不能给予不超过250mL/h(1.5小时内最大375 mL)的液体,以通过干扰凝血和作为直接血液动力学效应的可能的压力增加来最大化其优点并减少其出血的缺点。
由于已证实对低血压非代偿性失血性休克的有害作用,可能最好避免使用晶体液。
2.1.3.哪种液体最好?
用于THR的液体应该与用于液体负荷试验的相同,并且我们将使用它作为桥接手段,直到出血的源头得到控制。
所有液体类型都已经过测试。
在液体负荷测试中使用的液体和在大循环中维持最低限度的足够的容积和压力以及解决和优化微循环功能所需的液体之间存在显著的差异,液体负荷测试是对小动脉门系统功效的测试,主要目的是增加大循环的容积。
在THR使用的液体的类型和数量是相关的,因为每种类型都有其优点和缺点。微循环流动由两个主要因素维持:间接取决于上游压力的压力,以及层流的泊肃叶定律,其中粘度是最相关的变量,并且受晶体液的影响最大。
有充分的证据表明维持微循环功能的重要性,目的是通过使用具有特定特性和组成的液体来优化失血性休克中的灌注,尤其是血粘度,这是泊肃叶方程中支配微循环流动的最关键因素,而非胶体渗透压和胶体的性质。在小动物的实验中,高渗盐水(HTS)或合成的胶体组合(高渗、高粘溶液,如HTS、乳酸林格氏液或葡聚糖70与藻酸盐的组合,或聚乙二醇(PEG)结合白蛋白溶液)已被证明是微循环动力学的最佳选择。
从微观血流动力学和氧运输终点来看,血液具有不可替代的特性和功能。
就血液动力学稳定性而言,胶体优于类晶体,这有两个主要原因:(I)增加的膨胀/胶体渗透性能在微循环中特别有益,和(II)在院前,较小的所需体积有利于防止大循环中由于高压/高容积而导致的出血的持续或复发。然而,这些特性被许多标准胶体对凝血以及免疫反应和肾功能的损伤所抵消。
2.1.4.如果THR失败了,该怎么办?
这是一个治疗窗口,通过增加医源性抗利尿激素(ADH)来支持因ADH产生不足而即将崩溃的动脉系统。基本原理是加强小动脉阻力系统,直到赶到最近的外科设施。术前ADH优于去甲肾上腺素(NA),除非患者循环在进展中停止;然后,去甲肾上腺素的副作用消失,取而代之的是其联合的血管收缩变力和心动过缓作用。在术后重症监护室,如有必要,在更安全的情况下,在监测下,可以用钠替代或加入抗利尿激素。
失血性休克的代偿通过反射性交感神经介导的小动脉血管收缩,儿茶酚胺作用于α1受体。在某些阶段,对内源性儿茶酚胺的低反应性开始出现,标志着代偿失调,最终变成血管瘫痪,对外源性血管收缩剂也缺乏反应,标志着不可逆的休克。这很可能是由于缺氧打击了小动脉内皮细胞。
如果血管加压素无效且必须在ADH前停用,则应增加肾上腺素。
总的来说,除了节省血液需求之外,还缺乏显示血管加压药对发病率和死亡率有益的研究。
这种失败的主要原因是药物输送的时间选择不当。当心率在第三阶段和第四阶段之间的关键滞后期失效时,应给予血管加压药,目的是防止患者以远端微循环为代价失血。预计幸存者会出现一定量的缺血再灌注毒血症(IRT)。
如果低血压复苏对医源性血管加压药也不起作用,病人将很快进入IV期。
2.1.5.如果已知院前出血是静脉性的,该怎么办?
两种策略是可行的。
一种是提供总量相当于40% TBV的血液或其成分或液体。如果病人稳定下来,他们就被带到一个外科机构,只给予“保持静脉开放”的方式。在存在已知的缺血性心脏病(IHD)或脑血管疾病(CVD)的情况下,输血将是唯一的选择。
血液或血液成分通过中心静脉导管持续输入,直到出血源头得到快速控制。作为替代,可以插入两个14-16 G的外周静脉套管。虽然血液或其替代品会在大循环的连续性的解决方案中丢失,但它会灌注大脑和心脏,直到出血得到控制。可及性和成本使其在院外的使用受到严格的协议限制。
一个不好的问题是通过静脉输血会促进已经破裂的静脉出血处的失血量。
相反,如果患者没有变得稳定,并且对液体治疗没有反应,他们就进入了失血性休克的第IV期。
在这种情况下,连续输血和紧急送往外科机构将是一种选择。
第二种选择是“舀起就跑(scoop and run)”(译者注:紧急转运,对应短语:stay and play)送往最近的外科处置点,除了开放静脉通道之外,现场不给予任何治疗。
在一项具有里程碑意义的研究中,对躯干穿透伤低血压患者进行随机分组,一组根据经典的高级生命创伤支持(ATLS)冗长的指南进行标准液体复苏,另一组仅接受开放静脉开放但不输血,后者在存活率、发病率和住院时间方面得分较高。
Bickell的研究的基本信息已经被可预见地证实,长时间留在受伤现场,比紧急抢救和紧急运送病人到外科处置点所需的时间更长,这与死亡率之间有明显的关系。
上述策略也可以应用于已知为混合出血(静脉/动脉)的患者。
2.1.6.如果选择持续输血,在院前应该如何选择?
在控制出血源头的处置步骤中,补充失血量既是必须的,也是必要的。在Claude Bernard引入的“生理稳态”概念中,根据简单的基本逻辑和常识,如果出血时会发生失血,那么只有血液或血液成分需要补充。补充失血的目的是防止或减轻硬性缺血-再灌注现象,该现象与低氧血症期的水平和时长成比例。血液是血管系统的固有内容,因此负责血管的基本张力和动态压力以及心脏的容积和压力。除了特性的携带氧气的红细胞之外,血液还携带营养物质、炎症细胞和免疫细胞、激素以及凝血细胞和因子。原则上,全血是最好和最理想的选择,尤其是24小时内新鲜或流动的库存全血。或者,通常使用红细胞和血浆作为第二选择,红细胞和乳酸林格液作为第三选择。但血液仍然是不可替代的、天然的、个体程序化的、生命必需的携氧液体。它还携带其他重要气体,如CO2和一氧化氮(NO)。血液的重要作用还体现在它保持微循环流动的能力上,因为它具有完美的粘度,这是伯努利方程中最相关的变量。新鲜全血的另一个不可替代的作用是红细胞和NO在调节微循环中的作用。最后,全血可以加速血凝块的形成,而人工合成的液体会阻止或削弱凝块形成或稳定。然而,在院外使用血液的普遍存在的问题仍然是血液的可获得性。
新鲜全血、流动库存血或冷藏的低滴度O型全血(LTOWB)无需单独成分输血。就安全性和血液动力学性能而言,全血与血小板/浓缩红细胞/血浆比例为1:1:1的血液成分相比几乎相同。尽管该问题取得了一定的进展,但尚不清楚少量输注全血是否会降低血液制品的消耗量。由于保存了携氧能力和释放,流动的库存血或新鲜全血是最理想的,但冷藏的低滴度O型全血在储存两周时是否还能保持血小板健康和存活。
然而,尚无明确的证据表明,在院前给低血压患者输注全血或成分血有助于提高存活率。只有一项研究表明,与晚期休克患者不输血(晶体或无液体)相比,在手术室使用LTOWB可改善血流动力学,降低伤后早期6小时的死亡率,但现场死亡率无改善。该研究实际上因非LTOWB组中晶体液物质的负面影响和整体较高的病理学严重性而存在偏差。
院前环境优势的缺乏证实了最快的出血源头控制是生存率、死亡率和发病率的首要因素,而血液的补充作用主要是为了避免或预防缺血再灌注毒血症和全身炎症反应。如果出血源头没有得到控制,尽管这一点很容易也很普通,但是大量输血并不能挽救低血压、无法控制的进行性出血患者。高达40%的创伤中存在失血性休克;在12-34%的创伤和出血中,死亡是可以通过在1小时内从手术现场进行先进干预来预防的。大多数未干预出血的失血性休克患者在出血开始后2小时内死亡。在出现低血压的重度失血性休克患者中,较长的现场时间与死亡率之间存在关联。这意味着根据患者的生理状态和现场循环储备对患者进行分期对于晚期失血性休克的结果至关重要。
血浆是胶体的原型,是一种天然胶体,具有维持微循环的适当特性。通常情况下,新鲜冰冻血浆(FFP)作为多种凝血因子缺乏症的替代药物,对大出血患者(高达20–30 mL/kg BW)是有益的,特别是微血管出血(即渗出)、大量输血、弥散性血管内凝血(INR > 2)、严重烧伤、过度口服抗凝剂过量(华法林)和肝病凝血障碍。
院前血浆,同样,院前血液,无论是作为解冻的FFP (来源于AB型通用的献血者)、预解冻的血浆(特定血型)还是冻干的院前血浆,均未显示对失血性休克死亡率有益处。
未配型的液体血浆或冻干血浆现在已经取代了ABO配型的新鲜冰冻血浆,方便早期使用而不存在后续问题。然而,与不输注血浆或其他液体相比,没有令人信服的证据表明院前血浆可降低死亡率。
与以1.1:1的比例与红细胞和血小板组合的成分血相比较,其冻干形式的血浆和液体制剂形式的血浆解决了保存、储存和同时血液治疗的问题。
在动物模型中已经成功地测试了FDP的低体积喷雾干燥变体,其重构至其原始体积的三分之一,而不损害体内的促凝血特性,它更稳定,并且还保持了高胶体特性和高渗透特性。
在需要输血的情况下,它的优势在以下情况更能体现,仅在钝伤、创伤性脑损伤和转运时间大于20分钟。为什么只有钝伤?
在等容性炎症性休克(如脓毒性休克)中,血浆似乎有利于预防内皮损伤,并对微循环动力学产生影响。在一些钝性创伤中,例如,在具有少量失血的大型整形外科创伤中,会出现创伤后炎症反应。在这些情况下,炎症级联反应有更多的机会留在循环中,损害内皮和微循环。这一观察可以很好地解释为何输注血浆对钝性创伤有好处。
在脑创伤患者的优势可以很好地解释为输注血浆可以降低凝血病的事实,因此,这也是轻度或中度脑创伤患者血浆输注的适应征。
在延迟转运时,与输血相关可能是获益的贡献因素,原因可能是由于凝血得到增强。
当对没有活动性出血的患者过度输血时,血浆仍然有害,因为它会导致输血相关的循环超负荷和输血相关的急性肺损伤。循环超负荷、急性肺损伤以及红细胞、纤维蛋白原和血小板的稀释是其常见的不良作用。
尽管含有所有凝血因子(包括高于正常水平70%的纤维蛋白原),但也没有证据表明输血会促进凝块形成并增加纤维蛋白原,最终导致资源浪费。
在两项有关红细胞和血浆的研究中,由于在各种成分血使用的及时性方面的偏倚,以及对患者纳入标准和混杂因素(如低血压、气管插管、机械通气、血液动力学紊乱水平和各种院前输血的管理措施)的不恰当的描述,未发现对患者生存率有益处。
除非用作低血压复苏的液体或在烧伤、抗凝剂过量、DIC和肝病的特定情况下,输血在失血性休克中的应用是有争议的,并且可能是无效的、有害的,甚至是浪费的。
血小板以1:1:1的比例与血浆和红细胞一起输入。现在不可能预测输注的血小板的疗效。血小板功能障碍是一个问题,不能通过检测可靠地识别。血小板正常数值不排除凝血病,输血也不能保证血小板计数或其功能的恢复。此外,血浆或人工合成液体的稀释会影响它们在血凝块形成中的功效。
阿司匹林和其他抗血小板药物不会影响实体器官出血的结果,华法林或口服抗凝药物(OAC)也不会影响非脑损伤出血患者的结果。所有证据都证实凝血病不会影响结果,并且在休克中是一个不太重要的动态因素,无论如何,这些抗凝药物不应被视为损伤控制手术的一个标准。
有一篇关于脑创伤患者患者抗凝治疗管理的优秀综述。
在不伴有脑创伤患者的情况下,没有任何促凝血因子可以影响失血性休克的预后,因为它增加了轻度或中度脑损伤的干预阈值;但在有凝血缺陷的患者术后对血液或血液制品的需求减少以及增加非手术治疗的选择方面,促凝因子还是有其一定优势的。
没有任何促凝血因子或抗纤溶药物能够抵抗心脏泵的优势血液动力和出血后的血管压力(译者注:促凝血因子或抗纤溶药物不能单独止血)。
在需要特定凝血因子来恢复其凝血特征的患者中,在止血后给予冷沉淀;当纤维蛋白原活性测试显示存在纤维蛋白溶解时;出血时纤维蛋白原浓度低于0.8-1.0 g/L;不能用去氨加压素和浓缩的VWF/FVIII治疗的血友病(血管性血友病)患者。
氨甲环酸应仅用于轻度或中度脑创伤患者的失血性休克患者,无论患者是否有失血性休克,以防止血肿增大至干预阈值。
号称FFP/血小板/红细胞比例为1:1:1的固定方案可增加存活率是没有根据的,并且由于红细胞成分输血对存活率和血凝块形成的影响而有偏见,而不是因为解决了假设或事实上的凝血病本身。
晶体液作为一线即时的处理液,即使与红细胞和血浆一起使用,也只能通过凝血因子的血液稀释、血凝块的移动、血管舒张和压力增加而加重出血。Bickell等人在一项关于躯干穿透伤、低血压和未控制的血管损伤患者的里程碑式研究中指出,与标准液体复苏相比,如果在院前没有以标准方式给予液体,存活率增加,并发症减少,住院时间缩短。积极的基于晶体液的复苏策略也与心脏和肺部并发症、凝血障碍、免疫和炎症介质功能障碍相关,并发现与少量液体相比,积极的液体复苏与更高的凝血病、器官衰竭和脓毒症发生率相关。
仅在最近,ATLS已将失血性休克初始管理的建议类晶体液的量从之前的2 L缩减至1L。有趣的是,一项在血压正常和低血压休克患者中进行的< 500 mL晶体与> 500 mL晶体作为初始液体管理的研究没有影响低血压组的患者,但仅在血压正常组增加了患者死亡率。
ATLS之前推荐的2 L晶体负荷液体试验实际上是反生理的和有害的,特别是在不加选择地实施时,与不输液或液体限制性复苏相比,并没有增加患者存活率,反而增加了患者死亡率和术后并发症。
2.1.7.失血性休克III期的液体复苏管理简述
全血,1:1:1血浆、红细胞和血小板,1:1血浆和红细胞;重组DP(目前没有),液态或冰冻血浆,单独或单独红细胞;人造血浆;RL或血浆淋巴细胞,因此,根据休克进展中需求优先选择液体种类。
了解基本常识和患者的实际生理水平是至关重要的。
在失血性休克III期中,只要滴定低血压复苏(THR)起作用且氧合状况良好,最好不要使用血液或其成分来尝试稳定患者的病情。
所有的微循环研究都证实,在保持组织足够的氧和方面,粘度等变量比红细胞的携氧能力更重要。此外,目前还没有足够的证据表明院前应用血液或其成分能够增加其生存率。
因此,如果可以用合适的液体保持血粘度,且氧合状况良好,滴定低血压复苏(THR)有效,那么可以用常规的液体持续静点,直到应用外科手段控制出血源头。如果病人在失血性休克III期出现明确的缺血性心脏病或脑血管疾病,这种情况下血液的携氧能力可能会对复苏造成影响,此时针对性的应用血液或其成分可能更有价值。在这种情况下,在THR策略中使用定量的血液是合情合理的。
当静脉或混合出血需要持续输血时,有限的血液供应可能会对结局产生影响,此时紧急送往医院是最好的也是唯一的选择。
如果增加血管加压药的滴定低血压复苏(THR)失败,或补充血液、其成分或液体增加静脉回流没有让循环稳定,此时患者将进入即将到来的(心脏骤停)IV期。
2.2.院内管理
在院内,如果液体反应性证实持续的低血压和小动脉系统衰竭有关,应将患者带到手术室和/或介入放射科对出血部位进行快速处理。
2.3.出血是从何而来?
通常在明确的低血压休克中,没有时间进行影像学检查或其他检查,而临床诊断是事先确定出血来源的唯一机会。
肉眼可见的出血是不言而喻的,在医院也可以通过基本检查(胸部和骨盆X线)或高级检查(扩展超声-FAST,静脉造影CT扫描,或在选定情况下,诊断性腹腔灌洗或腹腔镜检查)等诊断方法确定出血部位。
快速临床评估;扩展超声-FAST用于胸腹部创伤,研究胸膜腔积气或失血,心包、肝周、脾周和子宫-直肠或膀胱-直肠袋的失血;根据临床情况对胸部、骨盆和颈部进行基本的X线检查是任何创伤中心或急诊室进行的常规检查。伴有血肿和气管损伤的颈部创伤也可以用超声检查出来。
时机至关重要,对当前生理状况的影响进行临床评估也是如此。对于失血性休克 III期或IV期的不稳定患者,任何诊断性CT扫描或介入血管造影都不应延迟明确和控制出血源的开腹手术,除非需要开腹手术后进行介入放射学诊治的危及生命的骨盆创伤(如骶骨骨折)。
血胸在临床上表现为呼吸音减低,叩诊浊音增加,并且语音震颤正常或减弱。超声是发现胸腔内出血的最快方法,在没有配备超声设备的地方可以采取诊断性胸腔灌洗。
腹膜后出血可以在无CT扫描,但有临床休克体征的情况下,通过扩展超声- FAST或DPL排除腹腔内出血(IAH)和胸部、四肢或颈部出血而得到诊断。
同样,钝性损伤导致的纵膈内闭合性出血,出血休克的临床表现,是心脏或大血管损伤的预兆,临床上已排除所有其他腔室可能的出血来源后可以诊断。
穿透性心脏创伤和纵膈创伤可能出现失血性休克合并心源性休克。心源性休克(CS)是一种与失血性休克类似的血管收缩型休克,例如当发现一个病人倒在街上,伴有严重休克特征,没有外部受伤迹象,且无法提供病史情况类似于后者。
当院外发现病人意识丧失并处于休克状态时,比如胸主动脉瘤破裂或夹层,大面积心肌梗死,大面积肺栓塞,或宫外孕破裂等任何情况都有可能导致出血。
当心源性休克与失血性休克重叠出现时,患者通常来不及到达医院。
3.危重/终末期休克,即将发生心脏骤停/卒中- IV期
除了避免进一步的损害并立即送患者进入手术室外,对于失血性休克的IV期目前还没有可推荐的治疗方法[图4]。
健康人通常发生在SBP≤60mmHg, MAP≤45mmHg, DAP≤40mmHg时发生心脏骤停/卒中。而患有充血性心力衰竭,左主干冠状动脉狭窄,急性右心衰竭,或高血压的患者可能在较上述指标更高情况下发生。
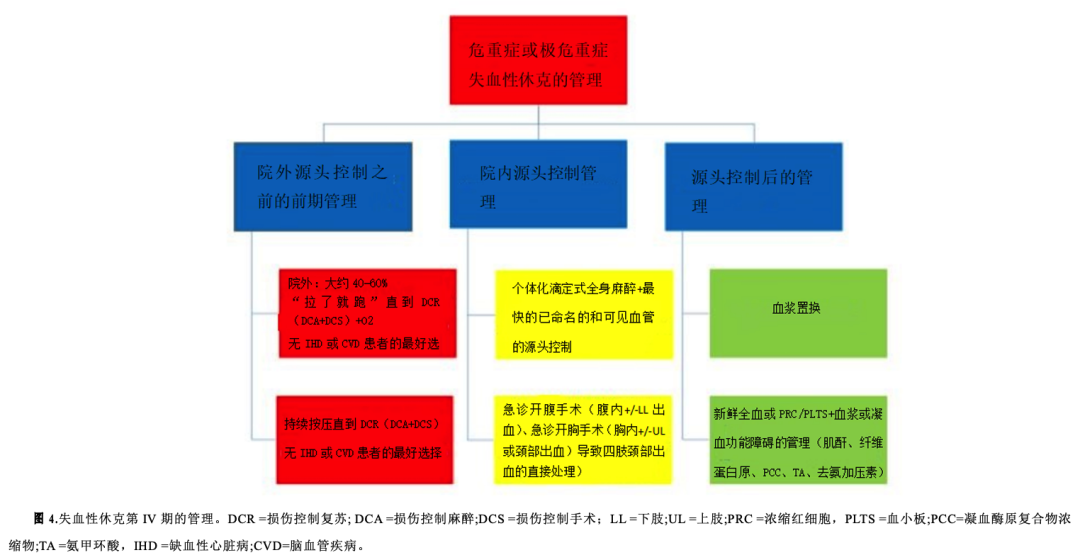
3.1.如何管理即将发生的心脏骤停(CA)
只有两个选择,分类的目的是通过打破维持病人生理的微妙平衡来避免病情恶化。
一种选择是由Bickell验证的“舀起就跑”策略,这种策略可以使病情更为严重的IV期休克患者发生转变。
Bickell等人进行的一项具有里程碑意义的前瞻性随机对照研究中,比较了穿透伤病人中立即液体复苏和延迟液体复苏的情况,研究发现延迟复苏的患者比在事故现场立即进行复苏的患者存活率更高。该研究纳入了年龄≥16岁、躯干穿透性损伤且收缩压(SBP)为90mmHg或更低的患者。干预措施是在院前进行的,立即复苏组在转运到医院过程中给予快速输注林格氏液,如果收缩压低于100mmHg,则入院后继续补液。延迟复苏组在途中或最初到达医院时未给予液体输注。
当患者表现出危急生理状况和即将发生心脏骤停的迹象时,救-生反射之间的平衡被拉伸到最大,而剩余的灌注不足(血液、氧气和基质)保持在一种易受微小变化或干扰变量影响的微妙平衡。任何干扰、破坏、打断或打破这种维持生命的平衡都会将病人推向不可逆的休克和死亡。因此,到目前为止,在没有液体/血液或外源性血管加压药的情况下,让患者的自然平衡机制在没有医源性干扰的情况下发挥其最佳状态,立即奔向最近的手术设施,直到快速/快速麻醉/手术来控制病源,这是最好的选择。
这种“舀起就跑”的选择适合于既往无缺血性心脏病或脑血管疾病的IV期休克患者。
第二种选择是一种合理的猜测,也是一把双刃剑;这取决于血液的可用性,就是连续输注PRC +/−血浆或全血;也就是说,首先尝试浓缩红细胞,如果意识、心脏监测或血流动力学没有积极的反应,则增加血浆,或从一开始就使用全血。血液比其他任何液体都能更好地保持微循环血流动力学,同时能够通过增加携氧能力来增加氧输送。
后一种选择适用于已知患有缺血性心脏病或脑血管疾病的患者。持续输注的全血或血液成分即便会顺着出血部位从循环中丢失,但输血经过微循环和补充的容量负荷仍可以保护心脏和大脑避免缺血性损伤。
在这种情况下,输液与血管加压药可以联合持续推注或输注。医源性血管加压药是为了预防心脏骤停。在这种管理期间,必须接受脑和心脏难以预测的进一步缺氧的风险。
3.2.用于预防失血性休克 的V期的近期策略,即失血引起的心脏骤停
复苏性主动脉球囊闭塞术(REBOA)应用空间很小,但在远离手术设施、预计转运时间较长、且证实腹腔内或下肢动脉出血的情况下是其明确的适应症。
由于实施球囊闭塞术需要5分钟的准备时间,并且最终需要在手术室进行处理,因此该手术仅局限于上述情况。此外,还有替代的手术方法是胸骨切开术(大约需要相同的时间)和开腹手术(更少的时间)。
当实施该方法时,需要实时关注压力监测和大规模IRT的预测。
最近提出的主动脉气囊泵与选择性主动脉弓含氧血灌注相结合是一个有趣的建议。尽管该方法比标准REBOA更具有生理性和针对性,但与之前的方法一样,它也提出了应用时机、适应症和时效性等问题。
体外心肺复苏ECPR(ECMO-CPR)已经成功地挽救了以心包填塞和/或大量血胸为表现的心脏和胸部大血管破裂导致的心脏骤停、肺损伤导致的呼吸衰竭、创伤后的肺栓塞需要手术或复苏等患者。
通过胸骨切开术进行体外膜肺氧合的成功,再次强烈的证明胸部切开术在心脏骤停中的关键作用,这也不可避免导致腹部损伤或四肢出血。
4.出血导致的心脏骤停-第V期
当失血量超过总血容量(TBV)40%时就可能发生心脏骤停(CA),大多数失血量约为总血容量的一半。而如果是高龄,高血压或心脏病患者,患者死于心肌梗死或中风,或死于静脉回流不足所导致的心脏骤停。在正常受试者中,失血量为总血容量的40%时,开始出现心脑缺血,失血量超过大约一半时出现心脏骤停。
在世界上大部分地区,死亡率仍然接近90%。在专注于创伤和高级领域研究的西方大学医院中,失血导致的心脏骤停的存活率约为10%,钝器伤的存活率为0-2%,胸腔穿透伤的存活率为10-15%,刀刺伤的存活率高达20%。
标准的心肺复苏会导致总血容量损失的速度增加,从而加速死亡。
因腹腔严重大出血(IAH)而进行的紧急抢救性开胸手术/胸主动脉交叉钳夹术(ERT/TACC)没有获得有意义的生存。ERT/TACC是在严格的胸部适应症下对心脏骤停患者实施的仅限于快进快出。
如果腹腔大出血发生在腔静脉或其主要输入静脉(股、脾、肾、髂、门静脉或肝后静脉),患者将因静脉回流不足而当场死亡。
如果腹腔大出血发生在大动脉,患者由于TACC导致的缺血-再灌注损伤(IRT)而将在数小时内死亡。
如果出血来源是静脉,旨在增加心室容量和压力的暂时夹闭,可与减少的静脉回流相抵消;如果出血源是动脉,则会导致IRT明显加重。
即使在高收住创伤病人和高ERT/TACC的有经验的单位的回顾性统计中,在对严重的IAH进行TACC的亚组中,在ICU中超过24小时的生存率很低,许多患者在4-16小时内死亡。
挤压开腹手术代替开胸手术有更高的生存几率,因为它避免了像紧急抢救性开胸手术在生理上精力、体力及时间的消耗过程。一个由两名经验丰富的护理人员组成的团队可以在几分钟内到达并处理ITH或IAH,一人用于开腹,两或三人用于出血源头控制,除外骨盆、肝后和肺静脉出血,通常所有部位处理最多耗费45分钟。
TACC在非心脏骤停患者的腹腔内大出血的应用会受到谴责。只有在胸腔内出血患者中才能发现TACC的幸存者。
一旦患者因失血过多而发生心脏骤停,这意味着患者已经失去了50%的总血容量。只有现场的抢救策略才能将他们从死亡中拯救出来。一旦患者脉搏消失,其发生转机的时间窗将非常短暂,脑缺血的临界时间仅为5分钟或更短,心脏缺血时间约为10分钟。
在成人中,大脑能耐受心脏骤停导致的缺血时间不超过4-5分钟,心脏大约10分钟。对于健康的心脏来说,还可有10分钟的挽救不稳定时间。心脏停止跳动后,大脑、心脏和身体其他器官进入一种被称为“停搏期”的边缘状态。这是一个终末阶段,死亡过程从这里开始。健康的心脏可以恢复节律的停顿时间不超过20-30分钟。
通过紧急抢救开胸术(ERT)抢救的穿透性胸部损伤的氧疗心脏骤停患者可持续长达30分钟。
只有插管或以其他方式氧疗且呼吸心脏骤停持续时间不超过5-10分钟的钝性胸部损伤中,才应进行复苏。
如果超过了10分钟的窗口期,并且现场目击了心脏骤停,则应尽可能的现场进行紧急抢救性开胸手术。对于钝性创伤的心脏骤停,如果插管在10分钟内到达,或未插管5分钟内到达,都应进行紧急抢救性开胸手术;否则,在钝性创伤中只有0.2%的存活率。如果在任何时候出现心搏停止,从心搏停止开始或持续减慢(<40次/分钟),如果患者处于PEA,大动脉搏动摸不到,或外周收缩压< 70mmHg,即无法监测到,就可以就地放弃复苏。如果患者获得复苏后自主循环恢复(ROSC),他们可以被送进急救室。
权威部门已经制定紧急抢救性开胸手术的终止标准。
在有生命迹象的胸部穿透伤中,心脏骤停30分钟后仍然可以通过紧急抢救性开胸手术进行复苏,存活率为10-15%,而刺伤的存活率高达20%。
采取开放的方法抢救创伤或非创伤性出血导致的心脏骤停是必须的。
体外胸/心按摩或按压通过增加每搏量而增加出血速度,并且加重机械损伤,进而加速患者死亡。无论是失血过多还是胸腔或腹腔血管破裂出现造成的心脏骤停,都不应进行标准的CPR。因为这样只会加速死亡。只有在10分钟内快速转运到达手术室内进行损伤控制性麻醉和紧急抢救性开胸手术 +/−手术患者才有可能存活。由于我们对这一边缘时期了解甚少,因此是否对心脏骤停出血的患者进行全身麻醉治疗是一个长期争论的话题。
在连续性的解决方案得到控制且有充足的促使CPR有意义且成功的Pmif后,体内外的CPR才会有效。
ERT/TACC可以在胸腔内出血或危及生命的心脏/肺门损伤引起的失血和心脏骤停中挽救生命。
规则很简单:(1)如果是腹腔内出血,就去腹部;如果是胸腔内出血,就去胸部——腹主动脉和主动脉弓也被夹住或更好。(2)如果首先不处理血管系统的连续性,静脉回流没有得到充分有效的恢复,使心脏重新开始泵血,那么出血引起的心脏骤停将无法逆转。(3)封堵和输血前切勿使用TACC。
备用的血管加压药的使用可以预防、延迟甚至有时可以逆转心脏骤停。在颈部底部被狮子咬伤或者在腹股沟褶皱下方横断股动静脉血管可使患者5-10分钟内死亡。
快速紧急抢救的前外侧开胸或胸骨切开术可以通过预先插入的中心静脉导管(CVL)或直接通过体内上腔静脉(SVC)/右心房插管控制源头、进行人工按摩,并在术中快速恢复静脉回流。
5.基本损伤控制复苏(损伤控制麻醉和手术)
5.1滴定-反应麻醉
治疗失血性休克全麻的目的是防止或加重低血压和低氧血症,使血压和氧合恢复正常,而不是加重或逆转有害的体温。
失血性休克患者插管期间出现严重低血压可导致心脏骤停和死亡。引起插管期间低血压的机制包括诱导药物引起的血管舒张,镇静剂引起的交感神经张力降低,以及正压通气引起的胸腔内压升高进而导致的静脉回流减少。
插管前已存在的低血压通常可以通过输血或血液制品、静脉输液和及时使用血管升压药物来纠正。对于插管过程中存在低血压风险的患者,应避免使用导致低血压的诱导药物。
熟练的手术麻醉是危重患者生存的必要条件。
在有或无气道保护下,使用氧和氯胺酮或半衰期及其起效时间最短的人工合成的短效阿片类药物瑞芬太尼实施全身静脉麻醉(TIVA)均可实现令人满意且安全的全身麻醉。
氯胺酮是非常适合麻醉诱导和维持的药物,兼有镇痛和镇静作用,会增加依赖于流量来增加氧输送的心脏的氧耗(VO2)和心率,在病人基本治疗方案中,它摄取氧输送(DO2)的75%。因此,它只能用于健康患者。它可用于正常或健康人失血性休克代偿期(轻至中度),但不能用于心率低于120次/分的冠心病患者。氯胺酮是唯一一种不抑制心肌、血管张力和气道张力的麻醉剂。由于这些原因,它作为诱导剂成功地用于户外战争场景,或仅用于非失血性休克且能够自主呼吸空气氧的TIVA患者。
在气道和出血源头得到控制且血压正常后可给予地西泮以缓冲氯胺酮的嗜神经、锥体外系反应和变时性作用,而甘罗溴铵推注可在不透过血脑屏障或增加心率的情况下控制唾液分泌的增加。筋膜、粘膜和皮肤对疼痛敏感,并引起自主神经反射增加和心动过速。琥珀酰胆碱可迅速治疗氯胺酮或瑞芬太尼引起的罕见喉痉挛。
氧气和阿芬太尼(起效最快的合成阿片类药物)组合或氧气和依托咪酯组合,由于它们的疗效和对心血管干扰很少,因此它们是最适合用于心脏病患者诱导的药物。与经典的外消旋混合物相比,氯胺酮的新型(L)、S(+)-异构体具有更小的时变性和致神经作用,有望成为危重症麻醉中的非常宝贵的药物,从而扩大了氯胺酮在心脏病患者中的应用。
丙泊酚具有降血压作用,由于其降低内分泌压力的特性,适用于轻度或中度的创伤性脑损伤失血性休克患者。
在晚期阶段,尽管依托咪酯和氯胺酮在失血性休克中优于丙泊酚,但可能不是更好的选择,一个是对肾上腺的抑制作用,另一个是致心动过速的作用。
在这样的危重患者中,必须使用氧气和合成阿片类药物进行诱导。患者的血流动力学越不稳定或越严重,就越应该使用氧气和合成阿片类药物进行简单而粗暴的组合来进行诱导和维持。
通过“按需TIVA”可以对全身麻醉进行维持,并且记住身体不同的进入部位遇到的疼痛敏感结构。只有皮肤切口和筋膜切口和牵拉,如浆膜腔,才会引起疼痛,此时需要足够水平的静脉麻醉剂。传统的麻醉剂和外科手术的时代已经结束,现在是我们走向实时定制个性化生理性修复的时候了。损伤控制麻醉,或自主控制麻醉,不管有无气道保护,可应用最短的半衰期和起效时间的氧气和氯胺酮或合成短效类阿片类药物瑞芬太尼进行安全、可靠地全静脉麻醉(TIVA)。
氧气和起效最快的合成阿片类药物阿芬太尼,或氧气和依托咪酯,最适合于诱导失血性休克或心脏病患者,因为它们对心血管功能干扰很小。
在脑创伤合并失血性休克的情况下,丙泊酚和氯胺酮连续静脉输注麻醉(CIVA)可控制颅内压和全身低血压。如果先进行躯干手术,则需要监测动脉压和颅内压。
5.2损伤控制手术
尽管10年来“损伤控制手术”(damage control surgery, DCS)一直应用于急诊手术而非创伤性出血手术,但早在上世纪初就被用于战争和选择性大手术,到20世纪90年代被广泛应用于创伤性出血的外科治疗。它描述了“仅处理撞击损伤”的行为,指的是在患者的生理状况稳定或改善后,在二次手术中完成。最终该术语被扩展到非创伤性急诊手术,如严重腹膜炎。
绝大多数外科手术干预有两个阶段:(1)针对病因/病源阶段:包括止血或控制出血,清除污染、感染、坏死、坏疽、缺血的组织或液体;(2)重建、恢复性的初期愈合阶段。
在一些外科手术中,损伤破坏阶段占主导,例如神经外科或胸外科手术;而其他手术普遍是纯粹重建阶段,例如血管,整形,矫形,颌面,或消化道。
创伤和急诊手术中存在严重生理紊乱的情况下,这两个阶段不会同时在初始、打击或导引手术中进行,为安全起见重建阶段可以推迟。
所有急诊治疗性手术的目的都是为了防止失血性休克或炎性(中毒性和感染性)休克造成的死亡。“出血源头控制”(即阻止活动性出血)和“源头祛除”(即清除污染、感染、坏死/缺血/坏疽的组织和液体)是我们在能力和功效的相同目的而进行干预的主要理由和原因。这就是所谓的损害控制手术(DCS)。
DCS概念最初的提出是由于错误的原因,即防止所谓的“致命三联症”(酸中毒、凝血功能障碍和低体温)的出现和进展,而事实上唯一的致命因素是酸中毒!凝血功能障碍并不影响创伤患者的死亡率;代谢性低体温是细胞缺氧程度的指标而不是原因,此外它并不影响创伤患者的死亡率。在过去的四十年中,创伤中的“致命三联症”的概念误导了创伤的临床研究,并使外科医生未领悟到DCS管理的真正关键所在。
5.2.1代谢性酸中毒
代谢性酸中毒(酸碱PH值、乳酸增多和碱剩余负值增加)普遍存在于休克中,是灌注不足、组织缺血缺氧导致的直接后果。此外,酸中毒在复苏过程中会抑制儿茶酚胺的反应,影响愈合,并改变Hb解离曲线。先前存在或伴随的肝病、饮酒、 和慢性阻塞性肺病可能会对乳酸水平增加存在潜在的干扰。PH值调整变化缓慢,这使得碱剩余负值(NBE)成为代谢性酸中毒的最佳和最可靠的实时监测参数。众所周知,pH <7.1和乳酸> 15-16 mmol/L对细胞内基本代谢过程的损害都是致命的[192],而NBE > 6-8 mmol/l是严重血流动力学/代谢紊乱的标志。
另一个可靠的标记物ScvO2是与细胞缺氧一致性最好的参数。在中央和外周静脉血中均有价值。它与NBE联合作为允许或避免打击操作重建阶段的可靠的预警信号来用于评估失血性休克的严重程度。
5.2.2 损伤控制外科(DCS)标准
创伤外科DCS的标准是在外科文献中引入相关术语时提出的,并不断进行重新评估。到目前为止,所有提出的损伤控制手术的适应症和阈值没有标准,因此这是一场不断变化的话题。在阅读过程中,一个人可能会在翻译中迷茫!
共同特性是什么?
应该使用概括性、直观性、真实性、科学性更强且具有共同特征,易于快速识别和快速应用的标准 [图5]。

源头控制的时间、难治性低血压、晚期组织缺氧/代偿性酸中毒和术中问题仍然是急诊或创伤手术中应用DCS的主要标准。其他具体的标准可以根据经验推断:具体来说,源头控制延迟,术前低血压,低血红蛋白或第一个样本血红蛋白下降,术前或术中损失1.5或2L的总血容量,术中低血压,特别是当脑创伤也同时存在时。
Asensio等人和Ordonez等人的研究提出了进一步的见解并证实了两个事实。当总血容量丢失30%时(平均体重70公斤的患者约1.5 L),毫无例外的会出现低血压,而根据经验在总血容量丢失更少,约20-30%范围内时,低血压是不稳定的,可能发生,也可能不发生。在不太紧急的情况下如果24小时内失血1.5 L通常需要开胸手术,间接证据表明总血容量丢失30%且持续低血压是血流动力学稳态的关键转折点。
对于一个普通成年人失血量2L约相当于总血容量的40%,这是危及生命的不祥征兆。对于孕妇来说,丢失总血容量的35%是低血压的下限,同时也是出现严重精神错乱的不祥征兆,此时病情危急,需要最迅速的进行干预。失血引起的心脏骤停通常发生在总血容量丢失一半的水平,而在心脏病患者中更少的血液丢失就会导致心脏骤停。
5.2.3 实施损伤控制外科(DCS)的可靠依据
降低创伤性出血早期死亡率的关键是尽早源头控制干预。
降低创伤性出血患者的中期发病率和随之而来的死亡率的是预防或缓冲经常发生的导致早期愈合失败(腹壁,吻合口)或后期MODS/MOF而引起二次打击的缺血-再灌注毒血症(IRT)。IRT决定了发病率和死亡率的第二次打击高峰(MODS/MOF),继发的肠道粘膜缺血导致屏障功能的破坏加剧,进一步引发了IRT、菌血症、内毒素血症,最终引发全身炎症反应(SIR)。这些反应和自我放大途径的自然结果是MODS/MOF和死亡。
自20世纪80年代以来,骨科医生在面临多发伤合并多发骨折患者骨折固定时机的困境时,就认识到创伤后炎症反应的相关性。结论是早期骨折固定是预防或减少创伤后不可避免的创伤后炎症反应的最好方法,特别是在没有出血的钝性骨折患者中。
在没有休克的钝性多发创伤的情况下,作为缺血、软组织损伤和局部污染/感染同步效应的IRT和SIR经常同时存在。
在伴有出血的创伤中,SIR的作用很小,因为炎症级联会随着出血而消失。
事实上,在没有失血性休克的主要骨科多发性创伤中,如果没有对重大骨折和软组织进行早期处理,SIR会导致早期的二次打击。同样,在伴有出血的钝性多发伤中,由于缺血、软组织损伤和局部污染/感染的同步效应,IRT和SIR经常并存,IRT是早期现象,SIR是晚期现象,而在伴有出血的穿透性创伤中,只有IRT可以作为早期的二次打击,这是缺血缺氧的效应,因为炎症级联的参与因子在循环中流失了。
只有当IRT的原因和影响效应没有进行源控制和源消除的处理时,才会发生继发性SIR,从而触发致命级联反应,导致MODS/MOF和死亡。
创伤后炎症反应或全身炎症反应(PTIR/SIR)在一个很少或没有出血的钝性创伤后会立即发生。甚至在心血管意外或大出血造成损伤之前,它就能当场杀死病人。它发生在血肿感染后。
IRT发生在创伤性出血早期或存在中毒性休克情况下。
IRT和SIR均可引起二次打击(MODS/MOF),累及肾脏,更严重的是累及肺(继发性急性肺损伤和缺氧性呼吸衰竭)。在第二次打击之前,尽管宏观循环变量是正常的,但有一段缓慢的、不衰减的、不停的、静默的、亚临床休克滞后期,此时基础的微循环仍在持续恶化。
很显然,因为它阻止了致命三联征的形成或恶化,就认为DCS降低了创伤与失血性休克的死亡率是一个误导的说法,这是几十年的对失血性休克分散的研究的结论。当存在严重生理紊乱的情况下,避免了具有非常高愈合失败风险(腹壁、肠吻合、软组织覆盖)的二次修复性、重建性一期愈合,从而避免、预防或缓冲了并发症及其相关死亡率。
微循环紊乱、低灌注和低氧血症对愈合的影响早已广为人知。在ICU中休克的病人应用儿茶酚胺类药物时,经常会增加更多的风险。在重建时期使用吻合器吻合可降低晚期吻合口失败的风险。
如果所有关于死亡和并发症的回顾性研究都旨在发现并关联IRT和SIR对愈合失败的影响,那么这里将会发现改善生存率的窗口期。回顾性研究应比较两组生理和病理状态类似或相似的创伤患者的发病率、死亡率和住院时间,其中一组采用DCS治疗,另一组采用一期重建。事实上,DCS对生存率的益处尚未被证实。然而,该策略带来益处必将在实践中被接受。
其原因是致命的三联征所带来的影响,相反,损伤控制手术的关键在于吻合口和腹壁愈合的能量衰竭,由于IRT、隐匿性低灌注和MODS对合成代谢过程的影响,禁忌进行一期修复性手术。对严重创伤所致死亡的分析可能会提示愈合失败是进展到死亡的主要事件,证实DCS有益的唯一方法是通过回顾性研究,比较生理上相似的采用一期重建治疗的患者组和采用DCS治疗组。
6.结论
探索式方法是基础。
从“临床试图适应生理学”到“生理学到临床”的方法转变,以及完全基于生理调节的管理是解决和研究不断发展的失血性休克的最佳途径。
大多数试图采用自上而下的视角进行研究的心理方法都存在缺陷和不足,特别是在人员和单位/中心/医院接触和专业知识因地而异、因操作者而异的主题中。所有的荟萃分析都存在相同的基本偏差:假装从冰山的尖端看到了海面下和冰山底部发生了什么。相关或关联并不一定意味着因果关系!如果一种似是而非的直接因果关系没有被首先证明的话,一个更深层次的、更严重的因素或纯粹因果关系和巧合,可能是相关的根本原因。
“一项研究的可信度可能取决于研究能力和偏见,同一问题上的研究数量,更重要的是,每个科学领域中研究的相关性的真实性与不真实性的比例。”如果在某一领域进行的研究规模较小,效应规模较小,被测试关系的数量较多且预选较少,在设计、定义、结果和分析模式上有更大的灵活性,而且有更大的经济、其他兴趣和偏见,那么研究结果就不太可能是真实的。对于当前的许多科学领域来说,公布的研究结果往往只是对普遍存在的偏倚的精确衡量”。
在这两种情况中,一是我们要么接受已建立和已观察到的血流动力学规律是绝对可信的,要么我们确定要故意忽视和抛弃它们,例如,与这些规律没有最低限度的联系的凝血,可能影响失血性休克的量和死亡率。经验的真理仍然是我们可接受的基础和目标,而且正如通常所见到的那样,它讲述了一个关于出血的更可靠的事实。也就是说,失血性休克的结果仅仅取决于事实和时期的主要流向:(1)在源头控制之前不恶化、稳定或改善患者的生理状态; (2)及时、尽早的源头控制; (3)血液和氧气补充; (4)在阶段(1)和(3)期间对氧气和温度的进行管理。没有其他因素会影响死亡率。
自一些医学先驱开始描述和研究失血性休克以来,IV期和V期低血压休克的死亡率约为40-50%和90%,这一点并没有改变。可见他们的见解仍然是真实的。
只有三种方法可以降低可挽救的失血性休克的死亡率和发病率:可靠地、及时地了解出血患者的心脏/循环储备,以及在达到临界容积和压力之前剩余和减少的总血容量的所需的时间;能迅速知道是动脉性的还是静脉性的还是混合性的出血,以及出血的部位;监测微循环功能而不依赖于大循环正常化。这才是研究应该关注的地方。几乎没有研究考虑到受门脉系统或一般生理反应对机体代偿能力的影响。
失血性休克的生理学分期是迄今为止最可靠、最实用的对失血性休克进行动态评估的方法,应用简单,依据充分,对确定滴定式低血压复苏(THR)和损伤控制外科(DCS)应用时机很有帮助。






