中南大学湘雅三医院团队发现肝癌发生新机制!
作为最常见的消化系统恶性肿瘤之一,肝细胞癌(HCC)已成为全球癌症相关死亡的第四大原因,是严重威胁人类健康的重大疾病[1]。 肝癌的发病过程涉及众多异常表达的基因及相应信号通路,目前研究已表明基因表达的RNA转录后调控异常是导致肝癌的重要机制[2]。 可变剪接(AS)是一种常见的转录后调控方式,通过对同一mRNA前体pre-mRNA的不同剪切及拼接,可以产生不同的mRNA剪接异构体,进而影响下游
作为最常见的消化系统恶性肿瘤之一,肝细胞癌(HCC)已成为全球癌症相关死亡的第四大原因,是严重威胁人类健康的重大疾病[1]。
肝癌的发病过程涉及众多异常表达的基因及相应信号通路,目前研究已表明基因表达的RNA转录后调控异常是导致肝癌的重要机制[2]。
可变剪接(AS)是一种常见的转录后调控方式,通过对同一mRNA前体pre-mRNA的不同剪切及拼接,可以产生不同的mRNA剪接异构体,进而影响下游蛋白产物的结构或功能,大大增加蛋白质功能的多样性[3]。
异常的可变剪接是肿瘤异质性产生的重要原因,同时在维持肿瘤增殖、迁移、侵袭以及治疗耐药中发挥重要作用[4, 5]。可变剪接过程主要由剪接因子调控,其中富含丝氨酸/精氨酸蛋白(SR)家族是主要的可变剪接激活蛋白,其异常表达可能在肿瘤发生发展中发挥不同作用[6]。
实际上,SR蛋白家族的不同成员,如SRSF1、SRSF2、SRSF3、SRSF5、SRSF9等已经被证实在肝癌进展中扮演着不同的角色[7-9]。然而,作为该蛋白家族成员之一的SRSF10在肿瘤发生中的潜在功能仍然不为我们所知。
近日,中南大学湘雅三医院曹科团队在著名期刊Journal of Experimental and Clinical Cancer Research发表了一项研究成果[10]。
他们发现SRSF10在肝癌中表达水平升高,并与不良预后相关。从机制上讲,SRSF10可通过调节细胞周期调节因子CDC25A的可变剪接,刺激肝癌细胞的增殖、侵袭,明确了SRSF10对于肝癌恶性表型的促进作用。

论文首页截图
研究人员首先基于公共数据库以及临床样本,分析了SRSF10在HCC及癌旁正常组织中的表达差异。
他们发现SRSF10在HCC中高表达,并与患者不良预后相关。他们还证实SRSF10可以促进肝癌细胞Hep3B和HepG2的增殖、侵袭等恶性生物学行为,并且细胞周期调节因子CDC25A可能是SRSF10调节的关键下游因子。
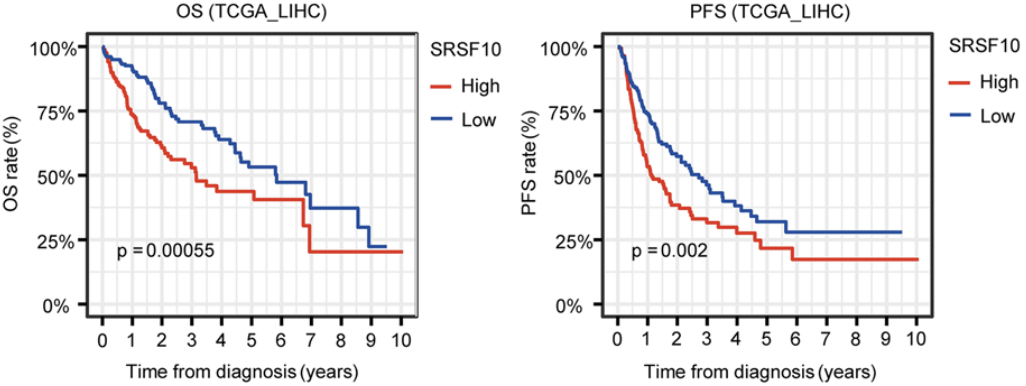
SRSF10与患者不良预后相关
至于SRSF10促进肝癌的具体作用机制。曹科团队发现,SRSF10可通过其RNA结合结构域与CDC25A pre-mRNA结合,发挥剪接作用,上调肝癌细胞中外显子6缺失的CDC25A mRNA亚型(CDC25A △E6)表达。
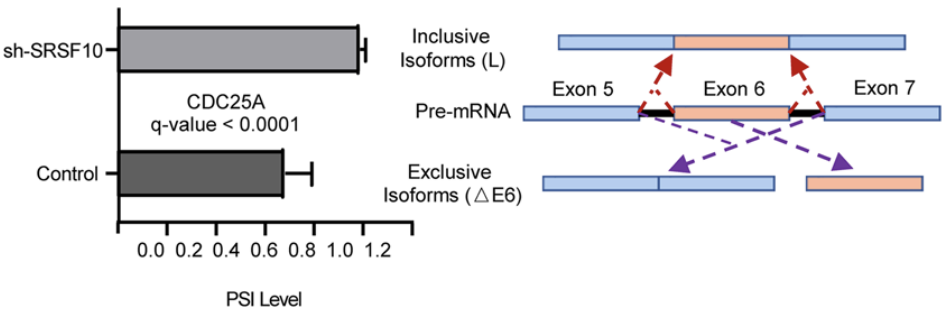
SRSF10调节CDC25A △E6亚型的表达
之前的研究表明,CDC25A是CDC25家族中的重要成员,具有磷酸酶活性,可以激活细胞周期依赖性蛋白激酶(CDK),在细胞周期转换及有丝分裂过程中起重要作用,是癌症治疗的潜在靶标[11]。
那CDC25A △E6亚型与未经剪切的longer CDC25A(CDC25A L)在生物学功能上有何差异呢?曹科团队在敲低内源CDC25A的肝癌细胞中分别回补CDC25A(△E6)及CDC25A(L),结果显示与CDC25A(L)相比,CDC25A(△E6)对肝癌细胞增殖、侵袭等恶性生物学行为的促进作用更显著。这表明CDC25A(△E6)具有更强的肿瘤促进作用。
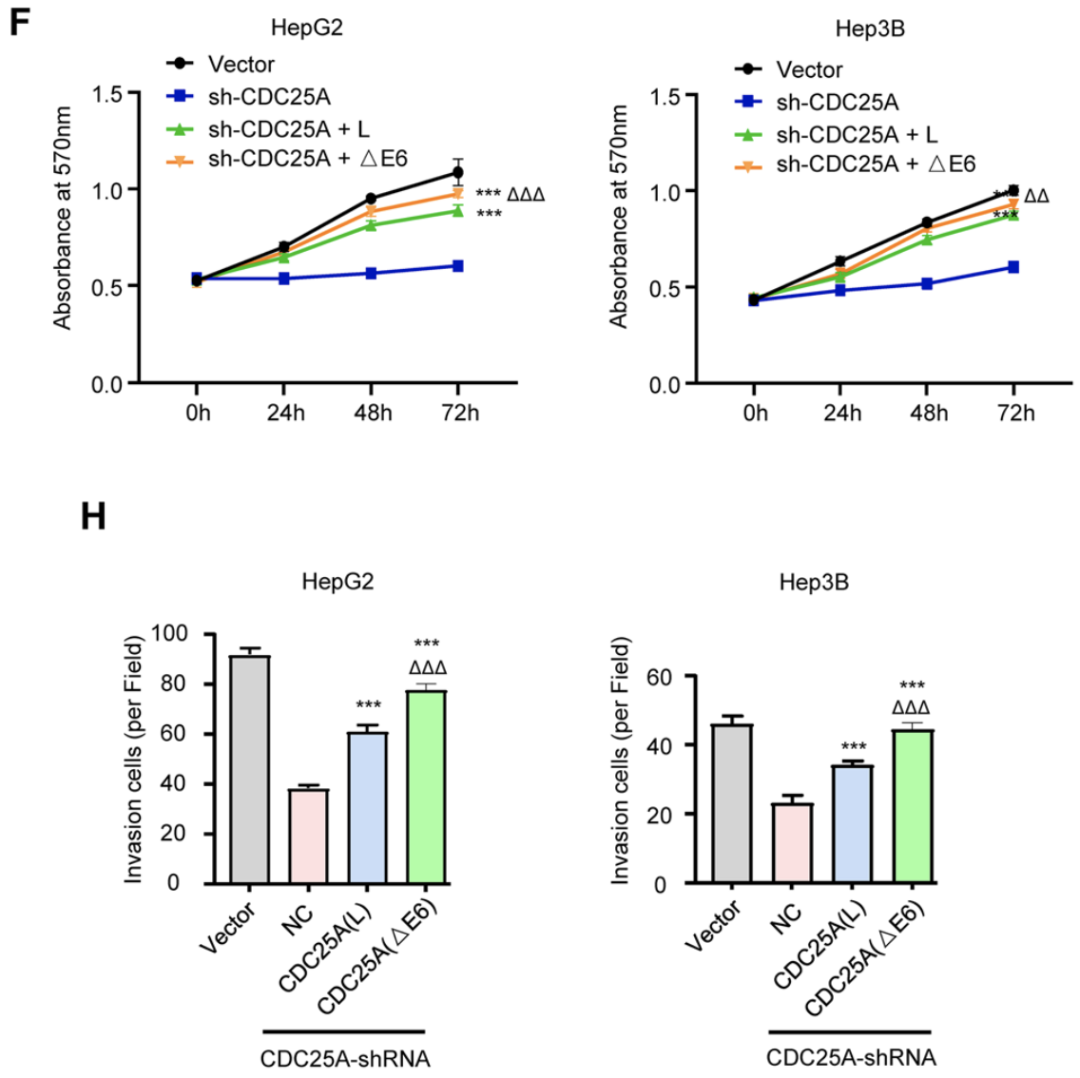
CDC25A(△E6)具有更强的肿瘤促进作用
与CDC25A(L)蛋白主要集中于细胞质不同,CDC25A(△E6)蛋白则主要在细胞核中表达,这是因为外显子6编码的蛋白区域(144-183aa)包含磷酸化修饰位点(S178),该位点表达的缺失导致CDC25A(△E6)磷酸化水平的下调并增加了其细胞核定位,从而发挥更强的细胞周期调节作用,促进肿瘤恶性进展。
此外,外显子6的缺失还会导致CDC25A(L)的两个泛素化修饰位点K150和K169的缺失,从而导致CDC25A(△E6)的泛素化修饰水平下调,蛋白质稳定性升高,表达水平上调。
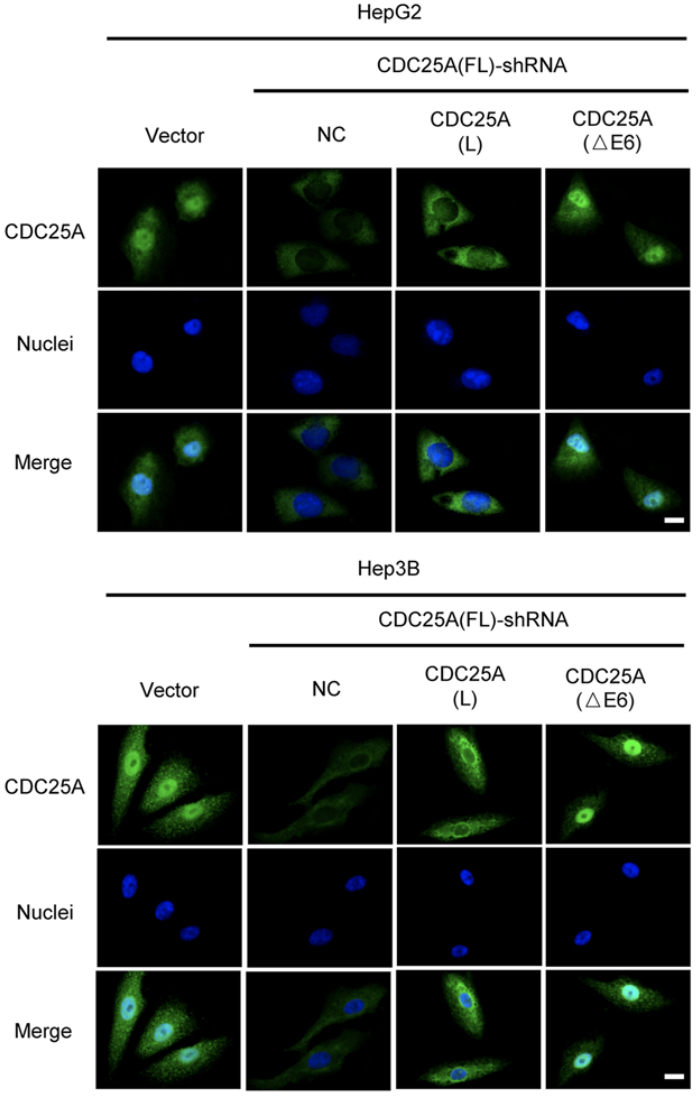
CDC25A外显子6表达的缺失影响其细胞定位
由此,研究人员证明,CDC25A外显子6的可变剪接,导致了泛素化和磷酸化位点的缺失,提高了CDC20A(△E6)的稳定性并促进了其在细胞核的积累,从而发挥了更强的促癌作用。
最后,研究人员在SRSF10过表达的细胞中分别敲低CDC25A(L)和CDC25A(△E6)。结果显示,与敲低CDC25A(L)相比,敲低CDC25A(△E6)对肿瘤的恶性表型具有更为显著的抑制作用。
同时,HepG2细胞的异种移植模型也显示:与CDC25A(L)相比,CDC25A(△E6)具有更强的促进肿瘤生长的作用。这进一步证明CDC25A的外显子6的剪切是SRSF10介导的HCC的恶性表型的关键下游机制。
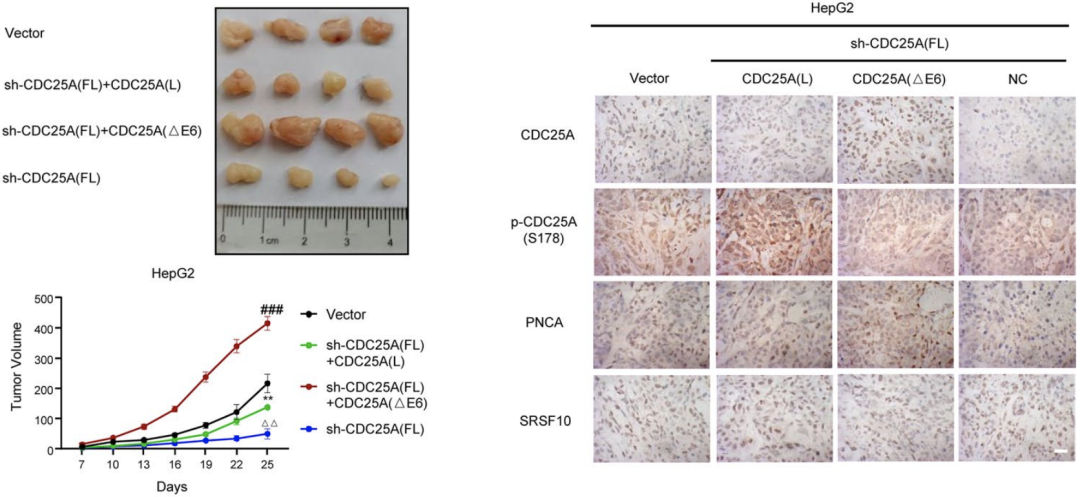
与CDC25A(L)相比,CDC25A(△E6)具有更强的促进肿瘤生长的作用
总的来说,本研究不仅证实了SRSF10对HCC恶性进展的促进作用,更重要的是发现了CDC25A的可变剪接亚型CDC25A(△E6),并证明其具有更强的促肿瘤作用。为CDC25A这一经典的促癌因子在肿瘤中的表达调控机制提供了新的见解,有助于推动该靶点相关抑制药物的开发及应用。






