儿童新冠病毒感染后,高烧抽搐,重点关注什么?
从全球来看,儿童感染新冠病毒后的风险是极低的,重症和死亡率都是非常低的。然而,对于婴幼儿,其并发症不容忽视。 据上海儿童医学中心的专家介绍,在儿童新冠病例中,时有急性坏死性脑炎出现,死亡率极高。往往病情发展十分迅速,甚至24小时内脑死亡。这些患者有新冠感染,高烧不退,但不一定有肺炎表现。 事实上,查询到中国台湾在开始感染时,也有类似现状。在今年夏天(2022年6月8日),中国台湾地区12岁以下儿
从全球来看,儿童感染新冠病毒后的风险是极低的,重症和死亡率都是非常低的。然而,对于婴幼儿,其并发症不容忽视。
据上海儿童医学中心的专家介绍,在儿童新冠病例中,时有急性坏死性脑炎出现,死亡率极高。往往病情发展十分迅速,甚至24小时内脑死亡。这些患者有新冠感染,高烧不退,但不一定有肺炎表现。
事实上,查询到中国台湾在开始感染时,也有类似现状。在今年夏天(2022年6月8日),中国台湾地区12岁以下儿童新冠重症累计39例,分别有17例脑炎、8例肺炎、3例败血症、4例哮喘,其中17人死亡。台湾成大医院小儿胸腔暨重症科主任王玠能表示,岛内确诊儿童出现多起神经学重症,特别是严重脑病变、急性脑炎、猛爆性脑水肿,这是境外经验较为少见的,医学界需探讨背后原因。
儿科领域的国际期刊《儿科杂志》(journal of pediatrics)也有相关报道。一项研究收集了巴黎地区12家医院转诊到necker-enfants malades医院的19例感染新冠后出现中枢神经并发症的儿童病例。该研究确定了19名有 sars-cov-2 感染史并表现出多种中枢神经系统(cns)炎症性疾病的儿童。他们的症状包括脑病、小脑共济失调、急性播散性脑脊髓炎(adem)、视神经脊髓炎谱系障碍 (nmosd) 或视神经炎。该研究显示,所有患者都有sars-cov-2暴露史或核酸检测阳性。在神经系统疾病发作时,8名儿童的新冠病毒核酸检测仍是呈阳性(鼻咽拭子)。58%的患儿(11人)脑脊液异常,74%的儿童(14人)出现mri异常。
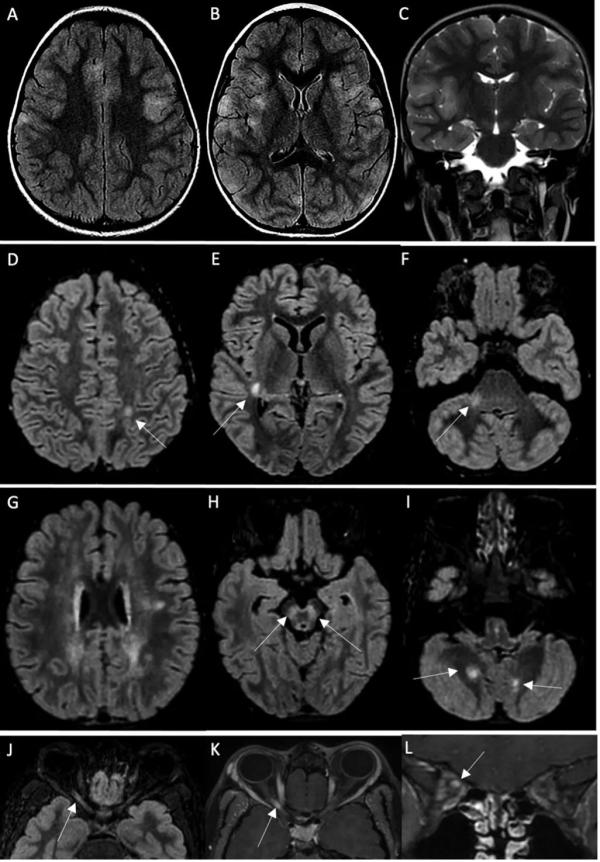
进一步检查最新的文献,印度也有类似报道。
2022 年 1 月,一名 2 个月大的男婴因癫痫发作到我们急诊科就诊。 几个小时前,他没有要求进食和睡觉。 然后,他被发现患有眼球滚动和异常运动的低渗症。 经检查,他有血流动力学不稳定。 患者的 PCR 鼻拭子呈 SARS-CoV-2 阳性。 大脑计算机断层扫描发现幕上层和幕下层、半椭圆形中心、岛状区域和脑干后部的低密度区域提示急性脑炎综合征。 复苏失败,入院 12 小时后死亡。 死后行腰椎穿刺,脑脊液(CSF)中白细胞和红细胞计数分别为〉<〉1个白细胞/mm3和400个/mm3。 Proteinoachia 为 2.33 g/L,glycorachia 为 6.9 mmol/L。 脑脊液中常见嗜神经病毒(包括 SARS-CoV-2)的 PCR 均为阴性。
从一开始就知道病毒可以通过血液进入中枢神经系统,因为我们经常观察到嗅觉丧失。 在脑尸检系列中,据报道出血是最常见的异常,其次是急性梗死和轻度至重度水肿病例 。 作者报告了检查、抽搐状态和意识障碍、眼球震颤和呼吸暂停。 在本例患者中,放射学检查结果未提示感染后过程,脑干低密度也未提示癫痫持续状态损害。 因此,我们假设 SARS-CoV-2 感染引起了暴发性脑炎。 在病程早期出现的神经系统症状和放射学发现支持这一假设。 我们无法评估 CSF 中是否存在这种病毒。
另外印度一项单中心研究观察了0-12岁儿童他们在 3 个月内有COVID-19感染的实验室证据和急性神经系统表现,并接受了磁共振成像 (MRI) 检查。 根据神经学发现将它们分为四组:急性脑炎综合征 (AES)、急性弛缓性麻痹 (AFP)、脑血管事件/中风,以及由无脑病的急性癫痫发作组成的杂项。 结果发现共有 19 名患有 COVID-19 感染相关神经系统表现的儿童被纳入研究。 AES 是最常见的神经系统综合征,占 47.36%,其次是 AFP,占 26.31%,心血管事件/中风占 21.05%。 癫痫发作是最常见的神经系统症状,占 62.15%,其次是脑病,占 42.10%,AFP 占 26.31%。 在神经影像学上,观察到的模式是 26.31% 的免疫介导的马尾神经根增强或 5.26% 的急性播散性脑炎,小的急性梗塞、海马和双侧丘脑信号改变各占 21.05%,微出血和白质脑病占 15.78%,以及 合并感染率为 5.26%。这项研究表明,在我们的研究中,癫痫发作和脑病是 COVID-19 感染最常见的神经系统症状。 感染后免疫介导的马尾神经根增强或急性脱髓鞘性脑脊髓炎样脑成像,其次是小的急性梗塞和海马/丘脑信号改变是最常见的成像模式。 我们在许多儿童身上发现了重叠的神经和 MRI 模式,这表明各种病理生理机制单独或协同作用。
在新西兰也报道了新冠病毒感染后出现脑干脑炎的情况。
在超过 4000 名住院的 COVID-19 患者中,有13 名具有神经系统症状并怀疑有神经炎症的患者。 在临床上,有8人被归类为神经系统症状与 COVID-19 之间存在可能/可能的关系。 在 6/8 的患者中观察到临床上独特的脑干和小脑症状表型。 由于我们在 3/5 的患者中发现 SARS-CoV-2 抗体指数呈阳性,表明特定的鞘内 SARS-CoV-2 IgG 产生,因此很可能与 SARS-CoV-2 有直接联系。
最新一篇文献进行了相关总结。
一、COVID-19合并脑炎或相关脑病儿童病例特点
1 儿童COVID-19合并脑炎或相关脑病的临床表现
15%~25% COVID-19或由COVID-19引起的MIS-C住院儿童出现不同严重程度的脑病,年龄范围包括婴儿及年龄较大的儿童,大部分既往无基础疾病,可在COVID-19症状出现数周后出现脑炎或同时出现COVID-19和脑炎症状。头痛是最常见的神经系统表现,其次是抽搐、嗜睡、易怒和情绪变化,局灶性神经体征包括言语障碍、步态异常等,部分病例进展迅速,可出现意识障碍、休克甚至死亡。我国台湾地区截至2022年9月8日共报道了30例COVID-19合并急性脑炎儿童病例,死亡11例。其中13例以病例报告形式可获取公开详细资料,其年龄为8个月至10岁,临床表现均以发热起病,其中11例有抽搐(8例为全面性发作,3例为局灶性发作);伴随症状以高血糖为主(5例);5例死亡,体温均超过39℃,其中2例超过41℃,病情进展迅速,抽搐后迅速出现意识障碍、休克,进展为多器官功能衰竭,导致死亡。
综上,COVID-19合并急性脑炎可以发生在各年龄段,包括婴儿及较大儿童,临床表现首先以COVID-19一般症状起病,包括发热、咽痛、呼吸系统症状(咳嗽、鼻塞、流涕等)、哮吼和胃肠道症状(腹痛、腹泻、呕吐等),随后出现重症前驱症状,包括超高热(体温>40℃甚至41~42℃)、意识不清(格拉斯哥昏迷评分量表≤12分)、持续昏睡、持续头痛、持续呕吐、步态不稳、癫痫持续状态等。同时表现出脑炎相关的临床表现,包括意识或行为改变、精神错乱、非自主性眼球运动、共济失调等,也可能出现上运动神经元症状(巴宾斯基征阳性)、锥体外系症状、角弓反张等。若处理不及时,病情可迅速进展,出现意识障碍、休克、呼吸衰竭、心律失常等,最终可导致儿童死亡。
2、儿童COVID-19合并脑炎或相关脑病的检查检验结果特点
检验结果方面,多篇文献提示COVID-19合并脑炎或相关脑病儿童的铁蛋白、乳酸脱氢酶等炎症指标明显升高,各个器官功能指标如氨基转移酶、肌酶、肌酐等均有不同程度的改变。大多数儿童脑脊液细胞数正常,脑脊液SARS-CoV-2阴性。我国台湾地区13例COVID-19合并脑炎患儿中[10-13],乳酸脱氢酶、白细胞介素、降钙素原等炎症指标明显升高。器官功能方面均有不同程度的受累,包括氨基转移酶、肌酶、脑钠肽、凝血功能等。其中2例患儿病程中出现弥散性血管内凝血。5例患儿完善脑脊液检测,4例正常,1例白细胞介素6明显升高,均未检出SARS-CoV-2。可见,根据流行病学史及神经系统症状,高度怀疑合并急性脑炎时,应及时完善铁蛋白、白细胞介素6、乳酸脱氢酶等炎症指标,完善凝血功能、肝肾功能、心肌酶谱等以评估器官功能损伤程度。
3、儿童COVID-19合并急性脑炎的神经影像学及电生理表现
诊断COVID-19合并脑炎最常用的方法是头颅磁共振成像(magnetic resonance imaging,MRI)、脑电图和头颅计算机断层扫描(computed tomography,CT)。最常见的MRI表现分别为脑白质高信号、颞叶高信号和胼胝体高信号。头颅CT多表现为脑白质低密度和脑出血。脑电图多为背景波减慢。我国台湾地区13例COVID-19合并脑炎患儿中,9例患儿完善头颅CT,结果发现3例局部轻度脑水肿,6例全脑水肿,其中1例脑干受累,1例出现严重的大脑及脑干水肿且双侧丘脑受累,即儿童急性坏死性脑病表现。由于急性脑炎起病急,病程进展迅速,大部分病例未能及时完善头颅MRI,仅3例患儿病情稳定后完善了头颅MRI,其中1例正常(病程第22天),1例皮质附近和脑室周围白质水肿,1例弥散加权成像示大脑半球多处信号异常(提示脑水肿)。2例患儿完善脑电图,均提示单侧痫样放电,伴背景波减慢。
COVID-19合并急性脑炎神经影像学主要表现为脑水肿,脑电图主要表现为异常电活动伴背景波减慢等。尽管头颅MRI可能是最优的影像学检查方案,但由于病情的急进性,大多数病例未能在急性期完善。有文献研究显示弥散加权成像可提供更多信息,能及时发现神经系统受损部位,表现为病灶区弥散受限,常提示预后不良。此外脑血流灌注成像如果出现局部脑血流量升高,提示脑电活动异常,考虑惊厥发作;反之,如果局部脑血流减低,提示局部灌注不足,预后不良。
4、COVID-19合并脑炎或相关脑病的合并诊断
文献报道多专注脑炎本身,并发症相关报道较少。但由于SARS-CoV-2感染是全身性疾病,脑炎可能仅为诸多并发症中的一项[30,41]。参照我国台湾地区13例COVID-19合并脑炎儿童病例的详细信息[10-13],发现除神经系统累及(暴发性脑干脑炎2例,急性脑炎4例,疑似脑炎6例,急性脑白质病1例)以外,该类患儿还容易合并其他脏器功能损伤,如急性肝炎(5/13)、急性肾损伤(3/13)、消化道出血(2/13)、肺出血(1/13)、弥散性血管内凝血(2/13)、凝血功能障碍(1/13)、休克(7/13)、心力衰竭(1/13)等。
5、COVID-19合并脑炎或相关脑病的治疗及结局
除对症治疗外,静脉注射甲泼尼龙/口服泼尼松和静脉注射免疫球蛋白是脑炎的常用治疗方案。我国台湾地区13例COVID-19合并脑炎患儿的治疗主要包括降颅压、抗病毒、控制惊厥、抗炎、器官功能支持等。其中6例应用甘露醇降颅压,12例给予瑞德西韦(remdesivir)抗病毒,7例应用抗癫痫药物,12例静脉注射或口服糖皮质激素,10例静脉注射免疫球蛋白,5例应用托珠单抗(tocilizumab),2例进行了血浆置换以减轻炎症风暴。此外还有6例应用血管活性药物,1例伴发暴发性脑干脑炎的儿童应用了亚低温治疗。最终5例患儿死亡,8例好转,神经系统后遗症情况尚不明确,待后续报道。
二、 经验及启示
1、COVID-19合并脑炎或相关脑病的早期识别
儿童COVID-19病例大多为无症状或轻症,其临床表现也以一般症状为主,包括发热、咽痛、呼吸系统症状等。急性脑炎病例,在上述前驱症状发生后,病情突然恶化,表现出神经系统症状。因此早期识别重症征象至关重要。包括体温升高明显(体温>40℃)、意识不清(格拉斯哥昏迷评分≤12分)、持续昏睡、持续头痛、持续呕吐、步态不稳、癫痫持续状态。若出现惊厥,和单纯性高热惊厥不同,如果发热为超高热(体温>41℃),且惊厥为局灶性发作,发作时间长,呈反复性,发作后30 min内意识无恢复,应警惕急性脑炎可能。
2 COVID-19合并脑炎或相关脑病的处理
如高度怀疑脑炎,应及时予吸氧、建立静脉通路、监测生命体征(心率、呼吸、血压等),给予降颅压、改善大脑灌注,并准备转至重症监护病房。我国台湾地区发布的诊疗指引,主要治疗方法如下。
2.1 降低颅内压
如怀疑患儿有颅内压升高,应及时完善头颅CT检查。首先给予20%甘露醇、地塞米松、3%氯化钠溶液减轻脑水肿,并密切观察神经系统症状变化。如出现顽固性脑水肿,可考虑气管插管过度换气或亚低温治疗。同时应限制液体摄入,以防止脑病变后引起的抗利尿激素分泌失调综合征所导致的低血钠。在维持基本血压的前提下,以适当的速度给予补液,并避免在极短的时间内给予快速大量静脉液体。若经上述治疗后病情仍持续进展,可考虑外科评估、行颅骨减压手术。
2.2 抗病毒治疗
我国台湾地区主要采用静脉注射瑞德西韦抗病毒治疗,然而我国大陆地区的一项多中心随机对照试验研究显示,瑞德西韦对重症COVID-19患者中没有显著的抗病毒效果[45],因此该药物在我国大陆地区仍未批准使用。目前奈玛特韦片/利托那韦片(paxlovid)已在国内紧急获批[46],其可降低SARS-CoV-2相关住院或死亡风险,可应用于抗病毒治疗,但适用年龄为12岁及以上儿童或成人,如需在较低年龄儿童超说明书用药,需要密切监测疗效及可能的不良反应。
2.3 抗炎治疗
推荐静脉注射免疫球蛋白和白细胞介素6拮抗剂托珠单抗。其适应证主要包括急性脑病变、急性无力性轻瘫麻痹、自主神经失调、急性心肺衰竭、败血症;急性脑病变伴有抽搐、合并意识障碍,如格拉斯哥昏迷评分≤12分,并排除单纯性高热惊厥。免疫球蛋白使用剂量为1 g/kg,每12 h 1次,共2 d;托珠单抗使用剂量为:体重<30 kg者为12 mg/kg,>30 kg者为8 mg/kg,单次静脉注射。
2.4 抗癫痫治疗
首选苯二氮䓬类药物,包括地西泮、咪达唑仑。若仍有抽搐持续发作,可考虑二线药物,包括丙戊酸钠、左乙拉西坦、拉考沙胺等。若进展至难治性癫痫,可考虑神经内科会诊,实行难治性癫痫治疗方案,并实时调整药物。若经上述治疗后病情仍持续进展,可考虑给予大剂量甲泼尼龙冲击治疗[30 mg/(kg·次),最大剂量1 000 mg/次,每日1次,共3~5 d]。
2.5 合并自主神经失调的处理
如患儿出现自主神经失调症状(出冷汗、四肢冰冷、高血压、高血糖、呼吸急促、心动过速等),应及时限制液体摄入,以70%维持量为原则,同时静脉给予米力农治疗。如病情仍持续进展,出现意识障碍、呼吸窘迫、心力衰竭、脑神经异常、频繁呛咳、矛盾呼吸、肺水肿、肺出血等,应及时给予机械通气治疗。如患儿有高血压表现时,不建议使用β受体阻滞剂、钙离子通道拮抗剂等降压药物。
2.6 合并心源性休克的处理
当心率逐渐下降,收缩压也逐渐下降,低于同年龄正常下限时,可认为进入心力衰竭期,此时血压可能迅速降低以致死亡。应及时应用血管升压素,以维持足够的血压,同时尽快区分患儿休克原因(心源性、神经性、感染性)。因COVID-19脑炎引发的休克通常是一种血管扩张性休克及心功能失调所致,建议优先应用肾上腺素,如周围血管阻力过高,可考虑应用多巴酚丁胺或米力农。若为神经性或感染性休克,则建议优先应用去甲肾上腺素,可加用血管升压素或肾上腺素。
三、预后及随访
急性脑炎病死率高,存活病例神经系统预后需要长期随访。国外研究数据显示,虽然大多数伴有神经系统症状COVID-19患儿的神经系统损害是一过性的,但有神经重症(即COVID-19合并急性脑炎)的患儿通常预后较差,病死率高达26%[27]。对于存活病例应长期随访,观察其有无神经系统后遗症,评估脑MRI、脑电图监测等。对于长期使用药物的病例,如抗癫痫药物使用的患儿,适时调整药物使用;对于伴有严重后遗症的患儿,评估患儿生活质量,必要时开展康复治疗。
小结
急性脑炎是COVID-19儿童急性神经系统重症并发症,早期识别、及时处理是改善预后的关键。本文通过总结、介绍COVID-19合并急性脑炎病例特点,以及我国台湾地区COVID-19合并急性脑炎临床治疗指南,以期为临床医生应对疫情期间可能出现的急性脑炎病例提供诊疗参考,对于改善儿童COVID-19重症病例的预后,具有重要意义。目前,全球COVID-19疫情尚未完全控制,COVID-19病例仍在不断增加,对COVID-19患儿的神经系统长期随访,并在此基础上进一步深入研究其神经损伤机制、探索干预的手段方法,显得尤为重要。
参考资料:
许普, 王来栓, 周文浩,新型冠状病毒肺炎儿童合并急性脑炎的临床特点及研究进展,中国当代儿科杂志,2022Vol.24 (12): 1301-1306 http://www.zgddek.com/fileup/HTML/2022-12-1301.htm
Abdelbari M, Tilouche S, Hannachi S, Bouguila J, Hannachi N, Boughammoura L.FulminantEncephalitisCaused bySARS-CoV-2in a Two-Month-Old Infant.Indian J Pediatr(IF:1.97;Q3). 2022 Nov 28:1. doi: 10.1007/s12098-022-04404-9
Negro A, Tortora M, Gemini L, de Falco A, Somma F, d'Agostino V.Neurological manifestations ofCOVID-19: a retrospective observational study based on 1060 patients with a narrative review.Acta Radiol(IF:1.99;Q3). 2022 Nov 30:2841851221138557.
Rastogi S, Gala F, Kulkarni S, Gavali V.Indian J Radiol Imaging(IF:0.59;Q3). 2022 Aug 30;32(4):510-522
Shamier MC, Crijnen YS, Bogers S, IJpelaar JW, de Vries JM, van der Jagt M, Spoor JKH, von der Thüsen JH, Schreurs MWJ, GeurtsvanKessel CH, Titulaer MJ.Brain stemencephalitisis a rare complication ofCOVID-19.J Neuroimmunol(IF:3.48;Q3). 2022 Nov 28;374:578007






