采用ADC药物Anetumab ravtansine治疗恶性胸膜间皮瘤的疗效和安全性
在2020年10月伊匹单抗和纳武单抗获批用作恶性胸膜间皮瘤的一线联合免疫治疗方案之前,培美曲塞和以铂类为基础的化疗是恶性胸膜间皮瘤唯一的一线治疗方案。迄今为止,恶性胸膜间皮瘤的二线治疗选择仍少之又少。 本研究是一项国际性、多中心、随机、开放标签的2期试验,旨在评估抗体-药物耦联物Anetumab ravtansine(一种全人源的抗间皮素抗体和毒性基团DM4组成的ADC药物)与长春瑞滨相比在恶性
在2020年10月伊匹单抗和纳武单抗获批用作恶性胸膜间皮瘤的一线联合免疫治疗方案之前,培美曲塞和以铂类为基础的化疗是恶性胸膜间皮瘤唯一的一线治疗方案。迄今为止,恶性胸膜间皮瘤的二线治疗选择仍少之又少。
本研究是一项国际性、多中心、随机、开放标签的2期试验,旨在评估抗体-药物耦联物Anetumab ravtansine(一种全人源的抗间皮素抗体和毒性基团DM4组成的ADC药物)与长春瑞滨相比在恶性胸膜间皮瘤患者中的疗效。
招募了年满18岁的经铂类+培美曲塞±贝伐单抗一线治疗后进展的不可切除的局部晚期或转移性过度表达间皮素的恶性胸膜间皮瘤患者,2:1随机分组,接受静滴Anetumab ravtansine(6.5 mg/kg,每21天疗程的第1天)或静滴长春瑞滨(30 mg/m2·周)治疗直到病情进展、不可耐受的毒性或死亡。主要终点是无进展生存期。
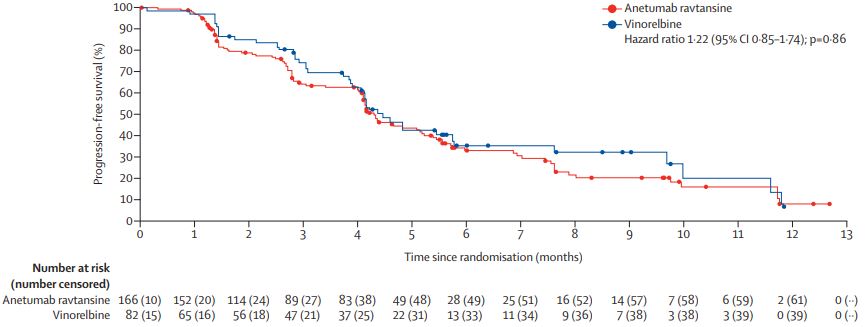
两组的无进展生存期和总生存期
2015年12月3日至2017年5月31日,共招募了589位患者,其中248位有过表达间皮素的患者被随机分至两组:Anetumab ravtansine组 155位,长春瑞滨组 82位。Anetumab ravtansine组和长春瑞滨组分别中位随访了4.0个月和3.9个月时,Anetumab ravtansine组和长春瑞滨组分别有105位(63%)和43位(52%)患者发生了病情进展或死亡,中位无进展生存期分别是4.3个月和4.5个月(风险比 1.22,p=0.86)。
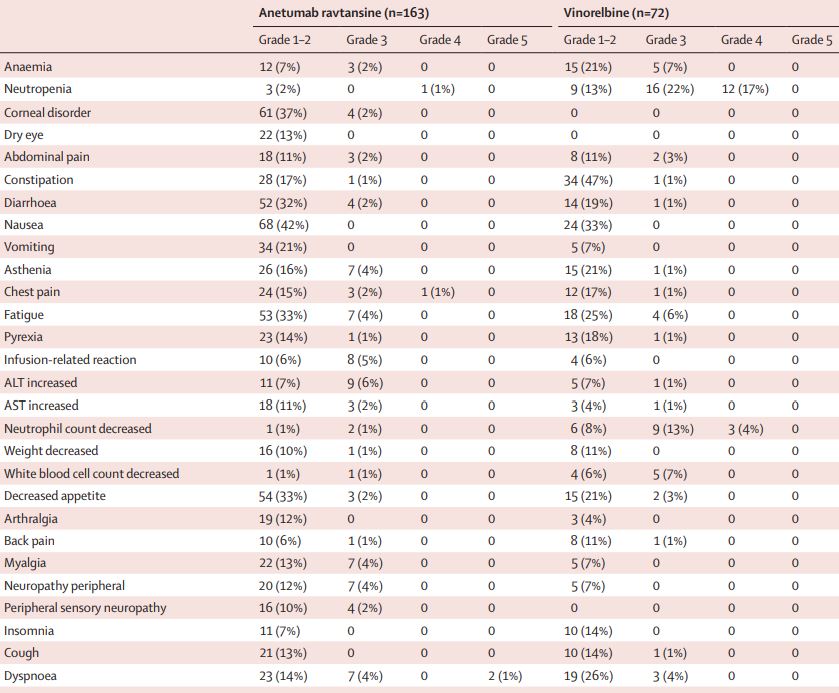
两治疗组的不良反应发生情况
最常见的3级及以上的不良反应有中性粒细胞减少(Anetumab ravtansine组 vs 长春瑞滨组:1% vs 39%)、肺炎(4% vs 7%)、中性粒细胞计数减少(1% vs 17%)和呼吸困难(6% vs 4%)。Anetumab ravtansine组和长春瑞滨组分别有12位(7%)和11位(15%)患者经历了严重的治疗相关的不良反应。此外,Anetumab ravtansine组有10位患者死于治疗相关不良反应。
综上,虽然Anetumab ravtansine在恶性胸膜间皮瘤患者中显示出了可控的安全性,但并不优于长春瑞滨。
原始出处:
Hedy L Kindler, et al. Anetumab ravtansine versus vinorelbine in patients with relapsed, mesothelin-positive malignant pleural mesothelioma (ARCS-M): a randomised, open-label phase 2 trial. The Lancet Oncology. April, 2022. https://doi.org/10.1016/S1470-2045(22)00061-4