降压新突破!醛固酮合酶抑制剂展现显著疗效,但需警惕这个潜在风险
血压是全球范围内的重大健康问题,影响着约13亿人,并且是心血管疾病的主要危险因素之一。尽管目前已有多种降压药物可供选择,但血压控制率仍不尽如人意。
高血压是全球范围内的重大健康问题,影响着约13亿人,并且是心血管疾病的主要危险因素之一。尽管目前已有多种降压药物可供选择,但血压控制率仍不尽如人意。醛固酮作为一种调节钠钾平衡的关键激素,在高血压的发病机制中扮演着重要角色。近年来,醛固酮合酶抑制剂(ASIs)作为一种新型降压药物,通过阻断醛固酮的合成来降低血压,显示出良好的应用前景。然而,由于现有研究多为小规模的Ⅱ期临床试验,其整体疗效和安全性仍存在争议。
2025年1月,Hypertension杂志发表了一篇题为“Efficacy and Safety of Aldosterone Synthase Inhibitors for Hypertension: A Meta-Analysis of Randomized Controlled Trials and Systematic Review”的文章,通过系统回顾和荟萃分析,综合评估了ASIs在高血压治疗中的疗效和安全性。

为了评估醛固酮合酶抑制剂(Aldosterone Synthase Inhibitors, ASIs)与安慰剂在高血压治疗中的降压效果和安全性,研究团队检索了MEDLINE和Embase数据库,筛选出截至2024年3月30日发表的相关随机对照试验。最终纳入7项随机对照试验,共涉及1440名患者,其中平均年龄为60.4岁,女性占比39%。研究人群包括原发性高血压、难治性高血压或未控制高血压患者。在这些试验中,78%(1130/1440)的患者接受ASIs治疗,22%(310/1440)的患者接受安慰剂治疗。另外,部分试验中还涉及ASIs单药或联合治疗(如与ACEI或ARB联合)的方案。本次分析涉及的ASIs包括osilodrostat、vicadrostat、lorundrostat和baxdrostat。研究的主要疗效终点是从研究开始到结束时的收缩压(SBP)变化,次要疗效终点为舒张压(DBP)的变化,而安全性终点则通过记录所有自发报告的不良事件的频率和严重程度来评估。
醛固酮合酶抑制剂显著降低收缩压和舒张压
Meta分析结果显示,与安慰剂相比,醛固酮合酶抑制剂(ASIs)在降低收缩压(SBP)和舒张压(DBP)方面表现出显著的疗效。具体而言,ASIs组的SBP平均降低6.3 mmHg(95%CI:-8.8~-3.8 mmHg,P<0.0001,I²=0%),而DBP平均降低2.2 mmHg(95%CI:-4.2~0.2 mmHg; P=0.03,I²=0%)。这一结果表明,ASIs在降低血压方面具有明确的临床应答,且在不同研究间表现出高度一致性,提示其在高血压治疗中具有潜在的广泛应用价值。
醛固酮合酶抑制剂的安全性分析
在安全性方面,ASIs的整体耐受性良好,未报告与治疗相关的死亡事件。不良事件的风险比(RR)为1.1(95%CI:0.9~1.2,P=0.3),表明ASIs与安慰剂相比并未显著增加不良事件的发生率。然而,ASIs组的高钾血症风险显著高于安慰剂组,风险比为2.5(95%CI:1.2~5.4,P<0.02)。尽管如此,ASIs组的血钾水平平均仅升高0.3 mmol/L,而安慰剂组无显著变化。这表明,尽管ASIs在降低血压方面表现出色,但其高钾血症的风险需要在临床应用中进行严格监测,尤其是在高剂量使用时。
剂量依赖性分析
亚组分析进一步探讨了ASIs的剂量依赖性。结果显示,随着ASIs剂量的增加,其对SBP的降低效果更为显著。在高剂量组中,SBP的平均降低幅度达到7.7 mmHg(95%CI:-10.4~-5.0 mmHg)。尽管这一趋势未达到统计学显著性,但提示ASIs的降压效果可能与其剂量相关。这一发现为未来临床应用中ASIs的剂量调整提供了重要参考,也为进一步研究其剂量-效应关系奠定了基础。
不同类型醛固酮合酶抑制剂疗效与安全性比较
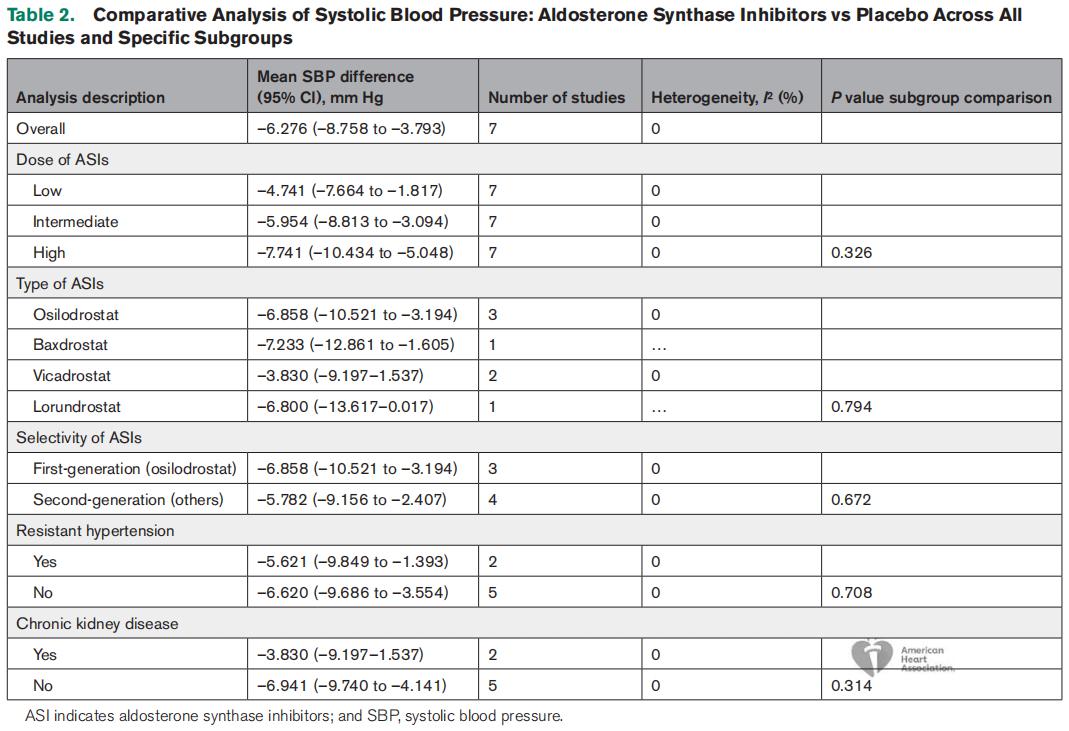
研究还对不同类型ASIs的疗效和安全性进行了比较。结果显示,无论是第一代ASIs(如osilodrostat)还是第二代ASIs(如vicadrostat、lorundrostat和baxdrostat),均显示出一致的降压效果和安全性特征。例如,osilodrostat组的SBP降低6.86 mmHg(95%CI:-10.52~-3.19 mmHg),而baxdrostat组的SBP降低7.23 mmHg(95%CI:-12.86~-1.61 mmHg,表1)。这表明,不同类型的ASIs在降压效果上具有相似性,为临床选择提供了多样化的选择。
面对不同患者群体的疗效一致性
此外,研究还探讨了ASIs在不同患者群体中的疗效一致性。结果显示,无论是难治性高血压患者还是慢性肾脏病患者,ASIs均显示出显著的降压效果。例如,在难治性高血压患者中,ASIs组的SBP降低5.62 mmHg(95%CI: -9.85~-1.39 mmHg),而在非难治性高血压患者中,SBP降低6.62 mmHg(95%CI:-9.69~-3.55 mmHg,表1)。这一结果表明,ASIs在不同患者群体中均具有良好的疗效,提示其在临床应用中具有广泛的适用性。
表1 醛固酮合酶抑制剂与安慰剂在所有研究及特定亚组中的收缩压比较分析
与依普利酮的比较分析
在一项事后分析中,研究比较了ASIs与依普利酮的疗效和安全性。结果显示,依普利酮组的SBP和DBP较基线进一步降低,但与ASIs相比,两者在不良事件和高钾血症风险上无显著差异。尽管如此,由于样本量较小,尚无法得出ASIs与依普利酮在疗效和安全性上的明确优劣结论。
总结
本综述对ASIs在高血压治疗中的疗效和安全性进行了系统的Meta分析。通过综合多项Ⅱ期临床试验的数据,不仅证实了ASIs在降低收缩压和舒张压方面的显著效果,还揭示了其剂量依赖性特征。尽管ASIs的总体安全性良好,但高钾血症的风险增加提示我们在临床应用中需要谨慎选择患者,并进行严格的监测。此外,本文还强调了ASIs作为一种新型降压药物的潜力,尤其是在难治性高血压患者中可能发挥重要作用。然而,由于纳入的研究多为小规模、短期的Ⅱ期试验,其长期疗效和安全性仍需通过更大规模、更长期的Ⅲ期临床试验来进一步验证。
扩展阅读
醛固酮的生理病理作用
醛固酮是一种由肾上腺皮质球状带分泌的盐皮质激素,主要通过促进肾远曲小管对钠离子(Na⁺)和氯离子(Cl⁻)的重吸收,以及增加钾离子(K⁺)和氢离子(H⁺)的排出,发挥潴钠排钾的作用。这种作用机制使醛固酮在血压调节中扮演关键角色。在生理状态下,醛固酮的分泌主要受肾素-血管紧张素-醛固酮系统(RAAS)的调控,同时心血管系统中独立存在的醛固酮合成系统也通过自分泌和旁分泌方式在局部发挥作用。
然而,醛固酮水平过高会导致一系列病理变化,包括心肌及血管间质纤维化、心室重构、血管壁增厚、大动脉顺应性降低和心脏功能恶化。此外,醛固酮还可阻断心肌细胞对儿茶酚胺的摄取,提高细胞外儿茶酚胺水平,加重心肌缺血。研究表明,醛固酮过高还会诱发白细胞浸润,导致冠状动脉损伤和心肌缺血性坏死,并通过激活炎症因子(如骨调素、单核细胞趋化因子和环氧合酶-2)引发血管炎症。
醛固酮受体拮抗剂的应用
醛固酮受体拮抗剂通过竞争性阻断醛固酮与其受体的结合,减少Na⁺的重吸收和K⁺的排出,从而增加钠和水的排出,减少尿量,发挥潴钾利尿作用。临床试验证实,血管紧张素转换酶抑制剂(ACEIs)或血管紧张素受体阻断剂(ARBs)与醛固酮受体拮抗剂联合使用,降压效果更为显著,尤其在顽固性高血压治疗中表现出色。此外,长期使用ACEIs或ARBs可能导致醛固酮水平升高,此时醛固酮受体拮抗剂可有效拮抗醛固酮对心脏结构和功能的不良影响,因此目前更推荐ACEIs或ARBs与醛固酮受体拮抗剂联合用于高血压和心力衰竭的治疗。
醛固酮合酶抑制剂的治疗机制
在病理状态下,醛固酮水平异常升高,尤其是在长期使用ACEIs或ARBs后,血管紧张素Ⅰ含量可能通过旁路合成血管紧张素Ⅱ,进而刺激醛固酮分泌。因此,从源头上抑制醛固酮的合成成为一种潜在的治疗策略。醛固酮合酶(CYP11B2)是催化醛固酮生物合成最后三步的关键酶,其与另一种同工酶11β-羟化酶(CYP11B1)的同源序列高达93%,两者均分布在肾上腺皮质区。CYP11B1参与皮质醇的生物合成,而CYP11B2则是醛固酮合成的关键酶。抑制CYP11B2可有效减少醛固酮的生成,从而减轻醛固酮的不良效应,成为治疗充血性心力衰竭、心肌纤维化和特定形式高血压的潜在方案。
醛固酮合酶抑制剂的临床应用与挑战
临床试验显示,螺内酯和依普利酮等醛固酮受体拮抗剂可显著降低充血性心力衰竭和急性心肌梗死后的致死率。然而,这些药物在拮抗醛固酮受体的同时,可能导致血浆醛固酮浓度升高,且无法拮抗醛固酮的非基因组活性。此外,醛固酮受体拮抗剂的常见副作用是高钾血症,需要密切监测患者的血钾水平。因此,直接抑制醛固酮生成的新化合物逐渐成为研究热点。
近年来,新一代醛固酮受体拮抗剂如Finerenone和Esaxerenone显示出更高的选择性和对醛固酮受体的亲和力,且在安全性方面表现出色,尤其适用于肾功能受损的患者。然而,与醛固酮受体拮抗剂相比,醛固酮合酶抑制剂的最大挑战在于其需要在高血压、心力衰竭或肾脏疾病中证明更好的疗效和耐受性。尽管如此,醛固酮合酶抑制剂通过直接抑制醛固酮的生成,不仅能拮抗ACEIs或ARBs引起的醛固酮水平升高,还能抑制靶器官中依赖或独立于醛固酮受体的醛固酮效应,为高血压治疗提供了新的方向。
参考文献
[1]MARZANO L, MERLO M, MARTINELLI N, et al. Efficacy and safety of aldosterone synthase inhibitors for hypertension: a meta-analysis of randomized controlled trials and systematic review[J]. Hypertension,2025. DOI: 10.1161/HYPERTENSIONAHA.124.23962.
[2]Wang YN, Guo YK, Zhong JF. Research progress in aldosterone receptor antagonists and aldosterone synthase inhibitors[J]. Shanghai Med, 2019, 40(1): 54-59. DOI: 10.6039/j.issn.1006-1533.2019.01.0056.



.jpg)


