采用卡博替尼联合纳武单抗治疗PCI难治性转移性尿路上皮癌
转移性尿路上皮癌 (mUC) 是一种高发病率的侵袭性很强的恶性肿瘤。目前,美国FDA已批准检查点抑制剂用于治疗经铂类化疗后进展的或一线治疗不能耐受铂类且PD-L1高表达的转移性尿路上皮癌患者。 本研究旨在评估卡博替尼联合纳武单抗(CaboNivo)在经检查点抑制剂治疗后进展的转移性尿路上皮癌患者中的疗效和耐受性。 这是一项I期的扩展队列研究,招募了既往接受过免疫检查点抑制剂治疗后进展的mUC患
转移性尿路上皮癌 (mUC) 是一种高发病率的侵袭性很强的恶性肿瘤。目前,美国FDA已批准检查点抑制剂用于治疗经铂类化疗后进展的或一线治疗不能耐受铂类且PD-L1高表达的转移性尿路上皮癌患者。
本研究旨在评估卡博替尼联合纳武单抗(CaboNivo)在经检查点抑制剂治疗后进展的转移性尿路上皮癌患者中的疗效和耐受性。
这是一项I期的扩展队列研究,招募了既往接受过免疫检查点抑制剂治疗后进展的mUC患者,予以卡博替尼 40mg/天+纳武单抗 3mg/kg·2周治疗,直到病情进展或出现不可耐受的毒性。主要终点是客观缓解率。次要终点包括无进展生存期(PFS)、缓解持续时间(DoR)、总生存期(OS)、安全性和耐受性。
共招募了30位患者,其中29位可进行疗效评估。中位随访了 22.2个月。大部分(86.7%)患者既往接受过化疗,所有患者都接受过检查点抑制剂治疗(中位7个疗程)。
缓解情况
客观缓解率达到了16.0%,包括1例完全缓解和3例部分缓解(PR)。4位获得缓解的患者既往接受检查点抑制剂治疗时,两例原发难治性的,1例获得了部分缓解,1例病情保持稳定。
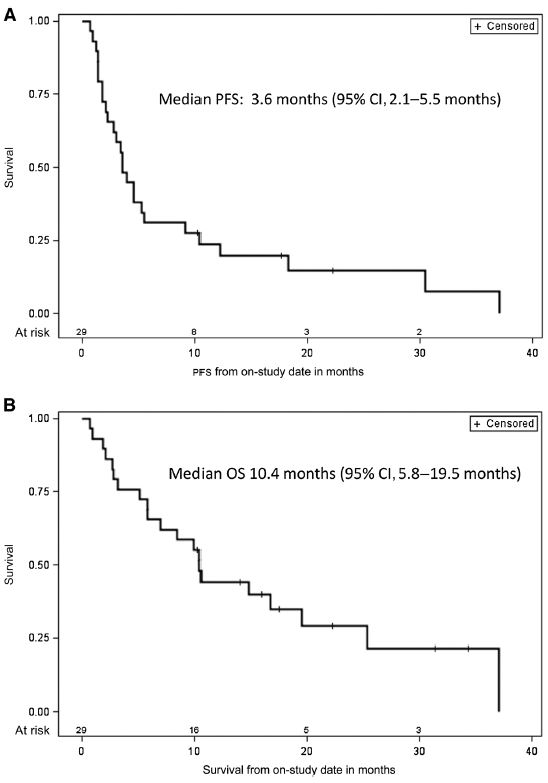
无进展生存期和总生存期
中位缓解持续时间是33.5个月,中位无进展生存期是3.5个月,中位总生存期是10.4个月。
该研究方案降低了免疫抑制亚群,如调节性T细胞 (treg) ,并增加了潜在的抗肿瘤免疫亚群,如非典型单核细胞和效应T细胞。基线时,单核髓系抑制细胞(M-MDSC)和多形核细胞MDSC百分比低、Treg细胞低表达CTLA-A和TIM-3、以及CD4+T细胞水平高均与更好的无进展生存期和(或)总生存期相关。
总之,卡博替尼联合纳武单抗在免疫检查点抑制剂难治性的转移性尿路上皮癌患者中有很好的抗肿瘤活性,而且耐受性良好。
原始出处:
Daniel M. Girardi, Scot A. Niglio, et al.Cabozantinib plus Nivolumab Phase I Expansion Study in Patients with Metastatic Urothelial Carcinoma Refractory to Immune Checkpoint Inhibitor Therapy. Clin Cancer Res February 10 2022 DOI:10.1158/1078-0432.CCR-21-3726





.jpg)


