早期非典型体征和岛叶低代谢可预测多系统萎缩患者的生存率
多系统萎缩(multiple system atrophy,MSA)是成年期发病、散发性的神经系统变性疾病,临床表现为不同程度的自主神经功能障碍、对左旋多巴类药物反应不良的帕金森综合征、小脑性共济失调和锥体束征等症状。由于在起病时累及这三个系统的先后不同,所以造成的临床表现各不相同。但随着疾病的发展,最终出现这三个系统全部损害的病理表现和临床表现。病理学上,这种神经退行性疾病的特点是-突触核蛋白
多系统萎缩(multiple system atrophy,MSA)是成年期发病、散发性的神经系统变性疾病,临床表现为不同程度的自主神经功能障碍、对左旋多巴类药物反应不良的帕金森综合征、小脑性共济失调和锥体束征等症状。由于在起病时累及这三个系统的先后不同,所以造成的临床表现各不相同。但随着疾病的发展,最终出现这三个系统全部损害的病理表现和临床表现。病理学上,这种神经退行性疾病的特点是α-突触核蛋白阳性胶质细胞质包涵体的积聚影响基底节、脑桥和小脑。
MSA的预后很差,据报道中位生存时间为6.2-10年。到目前为止,关于存活率的研究基本上包括临床数据,只有一个人认为18F-FDG正电子发射断层扫描(PET)代谢是非典型帕金森病患者生存的潜在预测因子。然而,脑PET可以通过强调特定解剖结构的代谢功能障碍来提供有关潜在病理生理学的信息,此外,18F-FDG正电子发射断层扫描目前被认为可以为MSA亚型的诊断提供额外的特征。本文在MSA患者队列研究中,目标是在临床和脑PET代谢特征中寻找生存预测因子。

生存曲线
在病程早期(平均3年,IQR 2-5)进行临床评估和脑部PET的疑似MSA诊断患者。采用标准化数据收集方法进行回顾性分析。脑PET代谢的特点是使用自动解剖标记图谱。应用Cox模型寻找影响生存的因素。使用Kaplan-Meier法估计生存率。建议使用多变量Cox回归分析中输入的重要变量,建立一个预测性的“风险评分”,分为低风险组和高风险组。本文还不能量化自主神经失调症状的严重程度,因为患者接受了治疗。SSRI治疗持续时间的数据是不完整的,因为大多数患者在第一次评估之前已经接受了治疗。因此,SSRI使用的最短持续时间可能被低估了。因此,无法从该估计中推断出可靠的相关性。
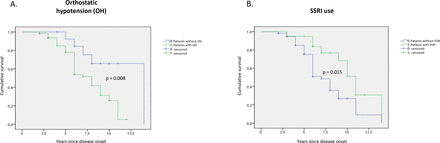
Kaplan-Meier法评价OH和SSRI治疗多系统萎缩患者的生存率
包括85名患者。总中位生存率为8 年(CI 6.64至9.36)。不良预后因素为直立性低血压(HR=6.04(CI 1.58~23.12),p=0.009),喘鸣(HR=3.41(CI 1.31~8.87),p=0.012)和左岛葡萄糖代谢低下(HR=0.78(CI 0.66~0.92),p=0.004)。良好的预后因素是诊断时间(HR=0.68(CI 0.54~0.86),p=0.001)和选择性5-羟色胺再摄取抑制剂(SSRI)的使用(HR=0.17(CI 0.06~0.46),p<0.001)。风险评分显示两组的中位生存期之间有5年的间隔(5年vs 10年) 年;HR=5.82(CI 2.94~11.49),p<0.001)。
总之,脑PET是有意义的预后评估,特别是在诊断是否左岛低代谢。此外,SSRIs是一种潜在的候选药物,以减缓疾病的进展。
GrimaldiS,BoucekineM,WitjasT, et alEarly atypical signs and insula hypometabolism predict survival in multiple system atrophy
Journal of Neurology, Neurosurgery & PsychiatryPublished Online First:23 April 2021.doi:10.1136/jnnp-2020-324823



.jpg)


