一文读透结直肠癌PD1免疫治疗神预测指标-微卫星不稳定(MSI)!
豪门的法眼,肯定是有它的过人之处的。 说起微卫星不稳定的家族,怎么能少的了它大家长微卫星呢,它虽然只是简单重复的DNA序列,由1-6个核苷酸组成,一旦出现异常,使错配修复基因(MMR,MismatchRepair)缺失,失去功能,发生突变,而且没法修复,微卫星不稳定性(MSI)就出现了,大大的增加了结直肠癌变的几率,有研究报道说有15%的结直肠癌跟它相关呢,更多见于右半结肠,跟发病相关就算了,还
“豪门”的法眼,肯定是有它的过人之处的。
说起微卫星不稳定的家族,怎么能少的了它大家长“微卫星”呢,它虽然只是简单重复的DNA序列,由1-6个核苷酸组成,一旦出现异常,使错配修复基因(MMR,MismatchRepair)缺失,失去功能,发生突变,而且没法修复,微卫星不稳定性(MSI)就出现了,大大的增加了结直肠癌变的几率,有研究报道说有15%的结直肠癌跟它相关呢,更多见于右半结肠,跟发病相关就算了,还关系到结直肠癌的遗传疾病筛查、治疗及预后。能不引起我们的”豪门“的注意吗?
那么微卫星不稳定是怎么被发现的呢?
那就不的不提到家族遗传性疾病“林奇综合征(Lynch Syndrome)”,也叫遗传性非息肉病性结直肠癌(Hereditary non-polyposis colorectal cancer,HNPCC),科学家们在研究这类疾病中发现超过90%的林奇综合征是由于错配修复基因(MMR)突变引起微卫星不稳定(MSI)而发生的。因此MSI/dMMR检测目前已经成为国际上筛选林奇综合征患者的重要诊断指标。MLH1缺失的MMR缺陷型肿瘤应行BRAF V600E突变分子和(或)MLH1甲基化检测,以评估发生林奇综合征的风险。听说子宫内膜癌、卵巢癌、胃癌、肺癌等对微卫星不稳定也有意思,但是还是不能竞争过结直肠癌这个“豪门”。
俗话说,“爱一个人,就要了解她的全部”,为了彻底的了解微卫星不稳定,“豪门”让科学家研究了可以检测它的不同方法
1
一、免疫组化(IHC)
该方法是通过使用相应抗体检测四种常见错配修复基因(MLH1、MSH2、MSH6和PMS2)在细胞核内表达的情况,明确是否存在错配修复功能缺陷。存在1种或以上蛋白表达缺失的,即为dMMR,相当于MSI-H;否则为错配修复蛋白完整(pMMR),相当于MSI-L/MSS。但是IHC检测容易受到抗体质量、检测过程(固定、染色)等因素影响。
2
二、聚合酶链式反应(PCR)
该方法是MSI检测的金标准,灵敏度高,特异性强。目前最常用的Bethesda标准检测5个位点,BAT-25、BAT-26、D5S346、D2S123和D17S250。结果出现2个或以上的不稳定为微卫星高度不稳定MSI-H,存在1个位点为微卫星低度不稳定(MSI-L),而无不稳定位点则为微卫星稳定(MSS)。但是PCR不能提供准确的突变基因,且实验周期较长。
3
三、高通量测序技术(NGS)
主要有两种方式,其一是通过全外显子测序检测TMB估测MSI状态,TMB高与MSI-H显著相关。另一种方式是通过选择一组位点的reads数目分布直接评估微卫星不稳定的程度(MSIsensor、mSINGS)。但目前NGS检测MSI尚缺乏统一的标准,且价格昂贵。
“豪门”有15%的发病率跟微卫星不稳定相关,躲它都来不及,干嘛还费尽心思地找它呢,因为啊,研究表明,MSI-H早期结肠癌(II/III期)具有独特的临床病理学和分子生物学特征,临床进展缓慢,淋巴结转移和远处转移较少,与非MSI-H型结肠癌相比预后相对较好。特别是在II期的MSI/dMMR结直肠癌术后患者中,单纯手术的5年生存率高达80%,化疗药物单药5-FU并未带来明显效益,我们2020年的CSCO指南就写的很清楚了。

再来看看我们2020年NCCN指南怎么说的,II期MSI/dMMR结直肠癌术后,观察就可以,连化疗都省了,对这部分患者是不是不幸中的大幸呢。

在Ⅲ期结直肠癌中,接受了术后辅助化疗的MSI-H/dMMR患者,预后是优于MSS患者的。
本以为他们的故事就仅限于此了,哪知,免疫治疗时代的到来再次激起了他们之间的火花。
早期的一些抗PD-1免疫治疗临床试验在转移性结直肠癌的治疗中并没有发现显著获益,后有研究将患者进一步细化,于2015年正式开启“豪门”与MSI的对抗时代。
先看看结直肠癌的后线免疫治疗。
KEYNOTE-016中,研究者发现dMMR的多种肿瘤均可从Pembrolizumab免疫治疗中获益,其中dMMR非肠癌患者的客观缓解率(ORR)为71%,而在晚期结直肠癌病例中,Pembrolizumab单药治疗在标准治疗失败的dMMR/MSI-H患者的ORR为40%,在pMMR患者的ORR为0。dMMR/MSI-H组所有患者均未达到中位无进展生存期(PFS)和总生存期(OS),而pMMR组中位PFS和OS仅为2.2和5.0个月。因此,该研究确定了dMMR/MSI-H是免疫治疗疗效的分子标志。
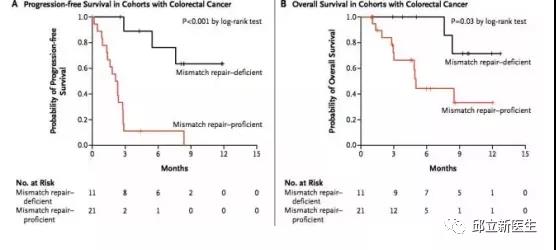
KEYNOTE-164和158研究证实,Pembrolizumab用于经治晚期MSI-H结直肠癌患者带来33%的ORR,且有长期生存获益。基于KEYNOTE-016、164及158等五项研究的卓越成果,2017年5月,FDA批准Pembrolizumab用于包含结直肠癌在内的所有具有MSI-H/dMMR的实体瘤患者的治疗。
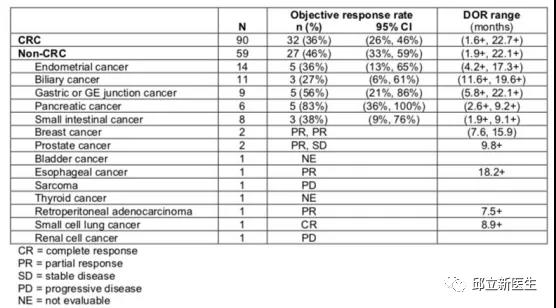
再往前看结直肠癌一线、二线免疫治疗
CheckMate 142研究,主要对Nivolumab为基础的治疗在转移性结直肠癌患者中的疗效与安全性进行了评估。结果显示,在一线治疗中,Nivolumab+Ipilimumab双免疫治疗的ORR为60%,BRAF突变患者的ORR比整体更高,为71%,当然该亚组的病例数较少,仅17例。二线以上治疗中,Nivolumab+Ipilimumab双免疫治疗在经治dMMR患者中的ORR为55%,Nivolumab单药用于经治MSI-H/dMMR 转移性结直肠癌患者,ORR为31%,1年生存率为73%,结果与Pembrolizumab类似。PFS和OS结果显示,一线治疗优于后线治疗,双免疫治疗优于免疫单药治疗。目前NCCN与CSCO指南均推荐免疫治疗用于dMMR/MSI-H肠癌患者。
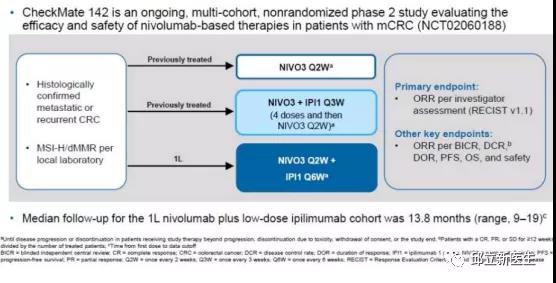
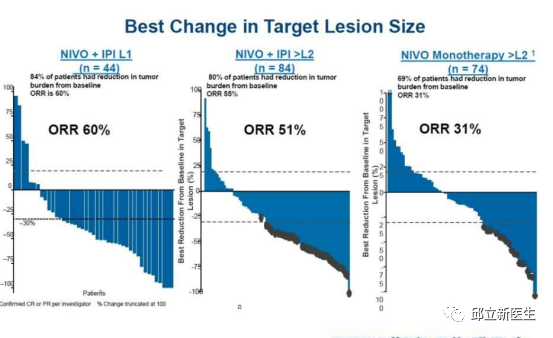
基于CheckMate 142研究,2017年8月1日,FDA加速批准 Nivolumab用于治疗12岁及以上,经氟尿嘧啶,奥沙利铂和伊立替康治疗后进展的dMMR/MSI-H转移性结直肠癌患者。
KEYNOTE-177研究,对270例dMMR的局部晚期结直肠癌或不可切除的转移性结直肠癌患者接受一线Pembrolizumab单药或化疗的效果进行了对比。这项国际、随机、开放标签的Ⅲ期临床研究以PFS和OS作为双重主要终点。目前该研究称PFS终点已达到,且PFS的改善兼具统计学意义和临床意义,另一终点OS数据尚未成熟,我们期待后续数据的更新。
另一项正在进行的COMMIT研究,主要对靶向+化疗、免疫单药、免疫+靶向+化疗的疗效进行对比,能否取得阳性结果仍有待观察。
紧接着就是新辅助免疫治疗了
2018年ESMO年会上报道的荷兰的NICHE研究,入组Ⅰ~Ⅲ 期结肠癌患者,dMMR和pMMR各7例,对Nivolumab+Ipilimumab用于术前新辅助治疗的效果进行了评估。结果发现,仅仅经过1个月的治疗[1次Ipilimumab治疗(d1),2次Nivolumab治疗(d1+15)],100%的dMMR肿瘤(7例)得到了明显缓解,4例患者达到了完全缓解,而pMMR患者则几乎没有出现缓解。该小样本研究提示在dMMR患者,新辅助免疫治疗带来的良好病理退缩,但是能否转化为生存获益,那就得看后续的进一步研究了,同时能否替代传统的手术治疗非常值得探索。
2020年ASCO更新了一项来自日本的VOLTAGE-A研究结果:研究纳入了MSS患者37人为队列A1和MSI-H患者5人为队列A2。结果显示,队列A1的37人中,11人达到了pCR(30%)。另外3人为TRG1级,即14例(38%)取得了重大病理缓解(TRG0-1)。另有1例患者达到cCR,进行等待观察,未行手术。队列A2的5人中,3人达到了pCR(60%)。截至2020年1月,A1和A2队列中位随访时间分别为22.5个月和6.6个月,MSS患者中2例出现局部复发,2例发生远处转移;MSI-H患者无复发。
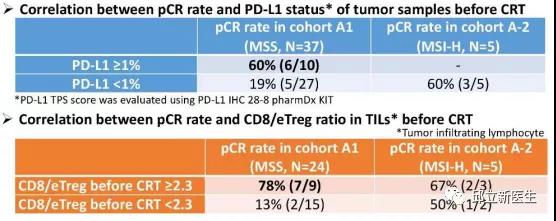
“豪门”想要全程对抗微卫星不稳定,怎么能放过术后辅助治疗呢?
术后辅助免疫治疗
ATOMIC研究,为了对结直肠癌术后辅助免疫治疗进行探索,将接受过手术与1个周期mFOLFOX6化疗后的Ⅲ期结肠癌患者进行微卫星状态的检测,并将其中的dMMR/MSI-H患者分为两组,分别接受后续的标准化疗或标准化疗基础上加用阿替利珠单抗。该研究尚在进行中,结果值得期待。
总之,微卫星不稳定与结直肠癌之间的故事还在上演,而且随着医学的不断进步以及临床研究的探索,它们之间的爱恨情仇会在癌症江湖中一直流传着,未来可期——
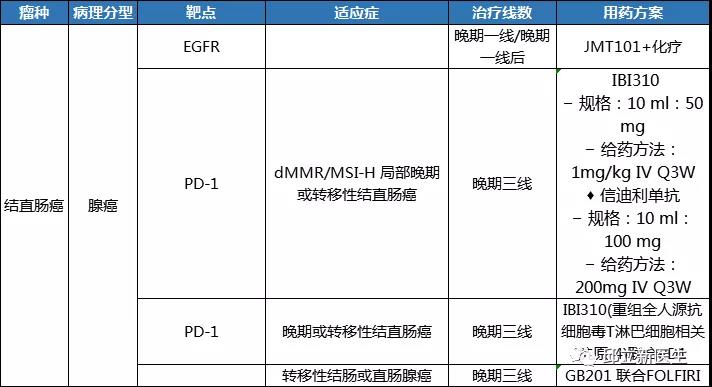
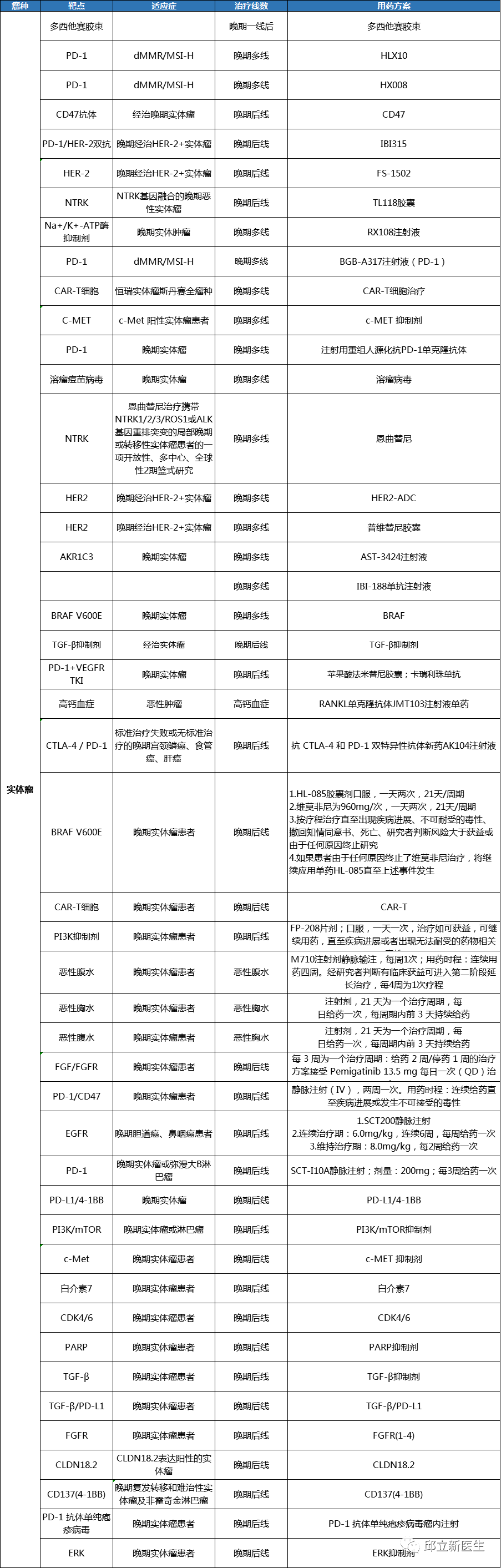
正在招募的临床试验(结肠癌 MSI-H SH实体瘤)
SIMPLE STYLE
结直肠癌