卵巢癌因其复发率高、死亡率高,被称为“妇瘤之王”。2020年,全球有约313,959人被诊断为卵巢癌。
铂类化疗药物,如顺铂和卡铂,通常是治疗卵巢癌的标准药物之一。然而,卵巢癌患者经多次治疗后,往往发生铂耐药。针对铂耐药复发卵巢癌(PROC)的治疗手段有限,预后极差。研究人员一直在寻找新的治疗策略和药物来克服耐药性,以提高患者的生存率和治疗效果。
然而,目前尚未有III期随机临床试验显示某种新疗法对于PROC患者的总生存期(OS)方面有益处。
本次2023年美国临床肿瘤学会(ASCO)年会公布了III期MIRASOL研究:mirvetuximab soravtansine对比研究者选择的化疗治疗叶酸受体α(FRα)高表达铂耐药的晚期高级别上皮性卵巢癌、原发性腹膜癌和输卵管癌的首次报告“Phase III MIRASOL (GOG 3045/ENGOT-ov55) study: Initial report of mirvetuximab soravtansine vs. investigator's choice of chemotherapy in platinum-resistant, advanced high-grade epithelial ovarian, primary peritoneal, or fallopian tube cancers with high folate receptor-alpha expression.”(摘要号:LBA5507)。Oncology论坛带你了解PROC的新治疗方案。

图1 ASCO现场
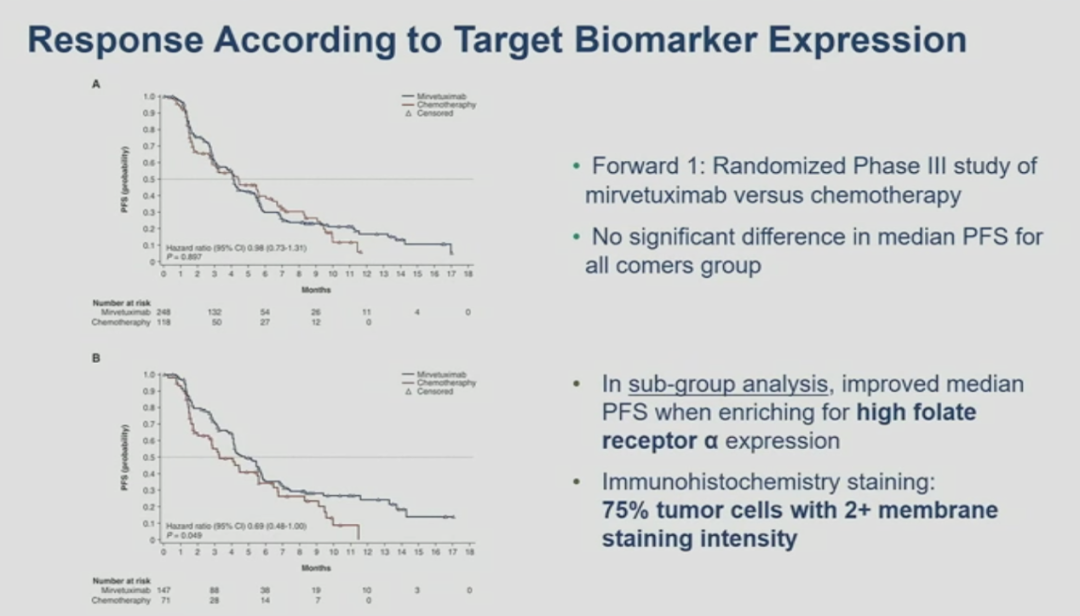
叶酸受体α(FRα)在大约90%的卵巢癌中表达,其中35%-40%的PROC肿瘤呈现出高水平的FRα表达(肿瘤细胞中有2+强度的阳性细胞占总细胞数的27%)。
Mirvetuximab soravtansine(MIRV)是一种抗体药物偶联物(ADC),包含一种与结合的FRα抗体、可切割的连接物和maytansinoid DM4(一种强效作用于微管的药物)。MIRV在贝伐珠单抗预治疗的PROC的单臂研究SORAYA中显示出32%的ORR和6.9个月的中位持续反应持续时间(mDOR),得到了FDA的快速批准[1]。
本次MIRASOL研究是MIRV在PROC治疗的再次尝试,并获得了较好的阳性结果。
MIRASOL是一项确认性的、随机的、全球范围的3期临床试验,旨在获得全球范围内的用药批准[2]。
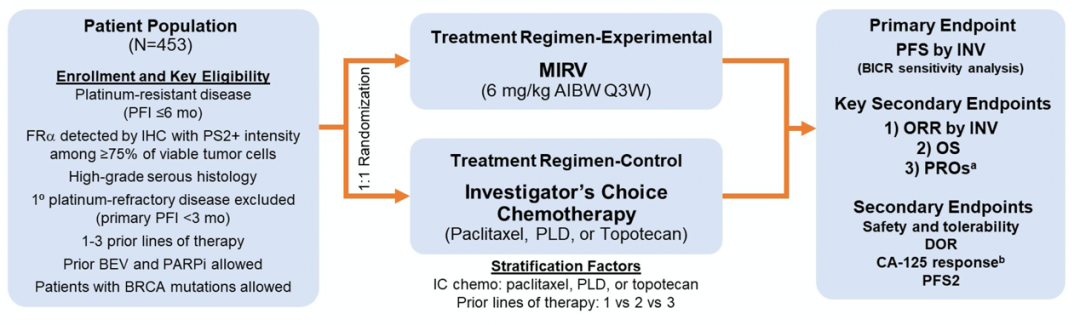
MIRASOL临床试验纳入了453名FRα阳性的铂类耐药性卵巢癌患者(晚期高级别上皮性卵巢癌、原发性腹膜癌或输卵管癌),FRα阳性定义为≥75%的肿瘤细胞免疫组化显示PS2+强度染色。入组患者既往接受过1-3线治疗,BRCA基因突变、既往接受过贝伐珠单抗和PARP抑制剂治疗的患者也可入选。
入组患者按1:1随机分组后,接受MIRV 6 mg/kg治疗(MIRV组),或者接受化疗(IC组)。主要研究终点为研究者评估的无进展生存期(PFS),关键次要终点为客观缓解率(ORR)、OS和患者报告的结果,按优先顺序进行分析;其他终点包括安全性和耐受性。对于PFS和ORR,进行了盲态独立评审委员会(BICR),以进行敏感性分析。
截至2023年3月6日,有227名患者被随机分配到MIRV组;226名患者被分配到IC组。中位随访时间为13.1个月。基线特征在两组之间平衡良好;14%的患者接受过一线治疗,39%的患者接受过两线治疗,47%的患者接受过三线治疗;62%的患者先前接受过贝伐珠单抗治疗;55%的患者先前接受过PARPi治疗。
该研究在主要和关键次要终点上达到了统计学显著的结果,包括PFS、ORR和OS。与标准化疗相比,MIRV组研究者评估的中位PFS为5.62个月(vs 3.98个月),研究者评估的ORR为42.3%(vs 15.9%),完全缓解(CR)率为12%(vs 0%)。
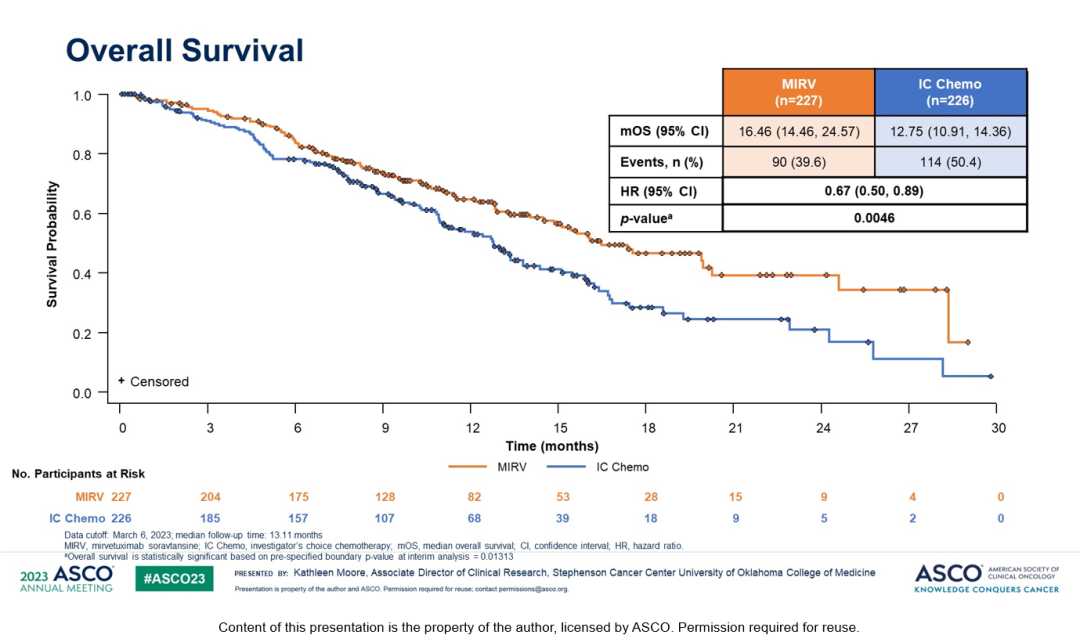
MIRV组对比化疗组的mOS为16.46个月 vs 12.75个月,这意味着MIRV组患者OS延长了将近4个月。
-
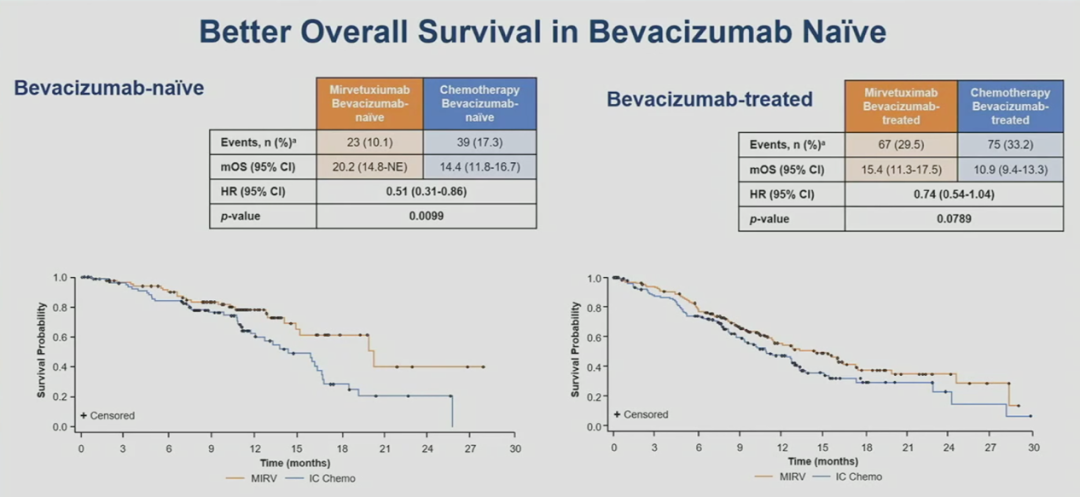
亚组分析中,既往接受过贝伐珠单抗治疗患者中(n=281),MRIV组对比IC组的PFS为4.4个月vs 3.0个月,OS为15.4个月 vs 10.9个月;
-
既往未接受过贝伐珠单抗治疗患者中,MRIV组对比IC组的PFS为7.0个月 vs 5.6个月, OS为20.2个月 vs 14.4个月。
图5 MIRASOL研究中根据既往是否接受过贝伐珠单抗分层的OS数据
-
在安全性方面,与MIRV相关的治疗副作用包括视力问题、疲劳、恶心、角膜损伤、腹痛、周围神经病变(称为外周神经病)、干眼症、腹泻和便秘。
-
与IC相比,MIRV组3级及以上的治疗相关不良事件发生率较低(42% vs 54%),严重不良事件发生率较低(24% vs 33%),由于治疗相关不良事件而停药的比例也较低(9% vs 16%)。
-
在MIRV组中,14%的患者仍然继续使用研究药物,而在IC组中仅有3%的患者。
但值得注意的是,MIRV引起眼相关不良反应的比例较高,如视野模糊、角膜病变和干眼症,需要与眼科医生配合减轻副作用。
ASCO大会邀请到了Memorial Sloan Kettering癌症中心的Róisín O'Cearbhaill教授作为讨论嘉宾。O'Cearbhaill教授提出了铂类耐药性卵巢癌领域的相关机遇与挑战。
对于铂类耐药性卵巢癌患者,深入研究其原发性和获得性耐药机制至关重要。原发性耐药机制的研究可以帮助我们了解为什么一些患者对铂类药物治疗就表现出耐药性,这可能涉及到肿瘤细胞自身的特征以及基因突变等因素。而获得性耐药机制的研究可以揭示在治疗过程中肿瘤细胞如何逐渐产生耐药性,并且有助于发展针对这些耐药机制的治疗策略。
在铂类耐药性卵巢癌患者中,抗原表达的异质性是一个重要的问题。某些患者的肿瘤细胞表达了高水平的抗原,如FRα,这使得他们对MIRV等靶向药物具有较好的治疗反应。然而,并非所有患者的肿瘤细胞都具有相同水平的抗原表达。因此,我们需要进一步研究抗原表达的异质性,确定抗原表达水平与疗效之间的关系,以便更好地选择哪些患者将从特定靶向治疗中获益最大。
在使用新型靶向药物治疗卵巢癌时,副作用的预防和控制是一个重要的考虑因素。对于MIRV这类药物而言,患者可能面临眼部相关的副作用。在治疗过程中,肿瘤医生需要与眼科医生紧密合作,共同关注并控制这些副作用。这包括向患者详细解释可能的副作用,采取适当的药物干预措施以缓解副作用,从而提高患者的生活质量和治疗依从性。
随着新靶点的发现与ADC及其他靶向药物的发展,未来将会有更多的靶向药物进入市场,我们也需要探索靶向药物与传统化疗药物的组合疗法,并确定具有最佳疗效的治疗方案。
O'Cearbhaill教授还提到,亚组分析显示,先前未接受过贝伐珠单抗治疗的子组中, MIRV组相对化疗组,OS提高较多,是否应该将MIRV应用于稍前线的治疗方案,也是临床医生值得研究的问题。
[1]. Matulonis et al. J clin Oncol. 2023:41(13):2436-2445
[2].J Clin Oncol 41, 2023 (suppl 17; abstr LBA5507)
卵巢癌因其复发率高、死亡率高,被称为“妇瘤之王”。2020年,全球有约313,959人被诊断为卵巢癌。
铂类化疗药物,如顺铂和卡铂,通常是治疗卵巢癌的标准药物之一。然而,卵巢癌患者经多次治疗后,往往发生铂耐药。针对铂耐药复发卵巢癌(PROC)的治疗手段有限,预后极差。研究人员一直在寻找新的治疗策略和药物来克服耐药性,以提高患者的生存率和治疗效果。
然而,目前尚未有III期随机临床试验显示某种新疗法对于PROC患者的总生存期(OS)方面有益处。
本次2023年美国临床肿瘤学会(ASCO)年会公布了III期MIRASOL研究:mirvetuximab soravtansine对比研究者选择的化疗治疗叶酸受体α(FRα)高表达铂耐药的晚期高级别上皮性卵巢癌、原发性腹膜癌和输卵管癌的首次报告“Phase III MIRASOL (GOG 3045/ENGOT-ov55) study: Initial report of mirvetuximab soravtansine vs. investigator's choice of chemotherapy in platinum-resistant, advanced high-grade epithelial ovarian, primary peritoneal, or fallopian tube cancers with high folate receptor-alpha expression.”(摘要号:LBA5507)。Oncology论坛带你了解PROC的新治疗方案。
oncology论坛
金宝搏网站登录技巧
肿瘤每日发送国内外肿瘤相关的前沿资讯、学术进展、病例讨论等内容,是肿瘤医生学习交流的平台。
40篇原创内容
公众号
叶酸受体α(FRα)在大约90%的卵巢癌中表达,其中35%-40%的PROC肿瘤呈现出高水平的FRα表达(肿瘤细胞中有2+强度的阳性细胞占总细胞数的27%)。
Mirvetuximab soravtansine(MIRV)是一种抗体药物偶联物(ADC),包含一种与结合的FRα抗体、可切割的连接物和maytansinoid DM4(一种强效作用于微管的药物)。MIRV在贝伐珠单抗预治疗的PROC的单臂研究SORAYA中显示出32%的ORR和6.9个月的中位持续反应持续时间(mDOR),得到了FDA的快速批准[1]。
本次MIRASOL研究是MIRV在PROC治疗的再次尝试,并获得了较好的阳性结果。
MIRASOL是一项确认性的、随机的、全球范围的3期临床试验,旨在获得全球范围内的用药批准[2]。
MIRASOL临床试验纳入了453名FRα阳性的铂类耐药性卵巢癌患者(晚期高级别上皮性卵巢癌、原发性腹膜癌或输卵管癌),FRα阳性定义为≥75%的肿瘤细胞免疫组化显示PS2+强度染色。入组患者既往接受过1-3线治疗,BRCA基因突变、既往接受过贝伐珠单抗和PARP抑制剂治疗的患者也可入选。
入组患者按1:1随机分组后,接受MIRV 6 mg/kg治疗(MIRV组),或者接受化疗(IC组)。主要研究终点为研究者评估的无进展生存期(PFS),关键次要终点为客观缓解率(ORR)、OS和患者报告的结果,按优先顺序进行分析;其他终点包括安全性和耐受性。对于PFS和ORR,进行了盲态独立评审委员会(BICR),以进行敏感性分析。
截至2023年3月6日,有227名患者被随机分配到MIRV组;226名患者被分配到IC组。中位随访时间为13.1个月。基线特征在两组之间平衡良好;14%的患者接受过一线治疗,39%的患者接受过两线治疗,47%的患者接受过三线治疗;62%的患者先前接受过贝伐珠单抗治疗;55%的患者先前接受过PARPi治疗。
该研究在主要和关键次要终点上达到了统计学显著的结果,包括PFS、ORR和OS。与标准化疗相比,MIRV组研究者评估的中位PFS为5.62个月(vs 3.98个月),研究者评估的ORR为42.3%(vs 15.9%),完全缓解(CR)率为12%(vs 0%)。
MIRV组对比化疗组的mOS为16.46个月 vs 12.75个月,这意味着MIRV组患者OS延长了将近4个月。
-
亚组分析中,既往接受过贝伐珠单抗治疗患者中(n=281),MRIV组对比IC组的PFS为4.4个月vs 3.0个月,OS为15.4个月 vs 10.9个月;
-
既往未接受过贝伐珠单抗治疗患者中,MRIV组对比IC组的PFS为7.0个月 vs 5.6个月, OS为20.2个月 vs 14.4个月。
图5 MIRASOL研究中根据既往是否接受过贝伐珠单抗分层的OS数据
-
在安全性方面,与MIRV相关的治疗副作用包括视力问题、疲劳、恶心、角膜损伤、腹痛、周围神经病变(称为外周神经病)、干眼症、腹泻和便秘。
-
与IC相比,MIRV组3级及以上的治疗相关不良事件发生率较低(42% vs 54%),严重不良事件发生率较低(24% vs 33%),由于治疗相关不良事件而停药的比例也较低(9% vs 16%)。
-
在MIRV组中,14%的患者仍然继续使用研究药物,而在IC组中仅有3%的患者。
但值得注意的是,MIRV引起眼相关不良反应的比例较高,如视野模糊、角膜病变和干眼症,需要与眼科医生配合减轻副作用。
ASCO大会邀请到了Memorial Sloan Kettering癌症中心的Róisín O'Cearbhaill教授作为讨论嘉宾。O'Cearbhaill教授提出了铂类耐药性卵巢癌领域的相关机遇与挑战。
对于铂类耐药性卵巢癌患者,深入研究其原发性和获得性耐药机制至关重要。原发性耐药机制的研究可以帮助我们了解为什么一些患者对铂类药物治疗就表现出耐药性,这可能涉及到肿瘤细胞自身的特征以及基因突变等因素。而获得性耐药机制的研究可以揭示在治疗过程中肿瘤细胞如何逐渐产生耐药性,并且有助于发展针对这些耐药机制的治疗策略。
在铂类耐药性卵巢癌患者中,抗原表达的异质性是一个重要的问题。某些患者的肿瘤细胞表达了高水平的抗原,如FRα,这使得他们对MIRV等靶向药物具有较好的治疗反应。然而,并非所有患者的肿瘤细胞都具有相同水平的抗原表达。因此,我们需要进一步研究抗原表达的异质性,确定抗原表达水平与疗效之间的关系,以便更好地选择哪些患者将从特定靶向治疗中获益最大。
在使用新型靶向药物治疗卵巢癌时,副作用的预防和控制是一个重要的考虑因素。对于MIRV这类药物而言,患者可能面临眼部相关的副作用。在治疗过程中,肿瘤医生需要与眼科医生紧密合作,共同关注并控制这些副作用。这包括向患者详细解释可能的副作用,采取适当的药物干预措施以缓解副作用,从而提高患者的生活质量和治疗依从性。
随着新靶点的发现与ADC及其他靶向药物的发展,未来将会有更多的靶向药物进入市场,我们也需要探索靶向药物与传统化疗药物的组合疗法,并确定具有最佳疗效的治疗方案。
O'Cearbhaill教授还提到,亚组分析显示,先前未接受过贝伐珠单抗治疗的子组中, MIRV组相对化疗组,OS提高较多,是否应该将MIRV应用于稍前线的治疗方案,也是临床医生值得研究的问题。
[1]. Matulonis et al. J clin Oncol. 2023:41(13):2436-2445
[2].J Clin Oncol 41, 2023 (suppl 17; abstr LBA5507)






.jpg)


