上皮性卵巢癌PARP抑制剂相关生物标志物有哪些?重点归纳!
卵巢癌是女性生殖系统常见的恶性肿瘤,发病风险因素包括家族史、遗传因素、年龄、体质量、子宫内膜异位症、未生育、激素替代治疗等。由于缺乏有效的早期筛查手段,患者就诊时多为晚期,在中国卵巢癌患者的5年生存率约为40%。
卵巢癌是女性生殖系统常见的恶性肿瘤,发病风险因素包括家族史、遗传因素、年龄、体质量、子宫内膜异位症、未生育、激素替代治疗等。由于缺乏有效的早期筛查手段,患者就诊时多为晚期,在中国卵巢癌患者的5年生存率约为40%。
近年来,随着聚腺苷二磷酸核糖聚合酶[poly(ADP-ribose)polymerase,PARP]抑制剂广泛应用于临床,有效地延长了晚期卵巢癌患者的无进展生存期。因此,对卵巢癌患者进行相关的生物标志物检测,有助于指导临床合理用药,改善卵巢癌患者的治疗结局。
PARP抑制剂相关的生物标志物
目前,与PARP抑制剂治疗相关的生物标志物主要有BRCA1/2基因突变、HRR基因突变、BRCA1/RAD51C启动子甲基化、HRD状态等。
1)BRCA1/2基因突变
BRCA1/2是重要的抑癌基因,对于维持细胞正常的生长增殖至关重要,也是维持细胞HRR功能最重要的基因。携带BRCA1/2突变的多种肿瘤对PARP抑制剂敏感,在SOLO-1研究中,携带胚系或体细胞BRCA1/2突变的晚期上皮性卵巢癌患者在初始治疗缓解后应用奥拉帕利维持治疗,相比安慰剂,患者复发或死亡风险下降70%,中位PFS延长3年以上。
明确卵巢癌患者的BRCA1/2胚系突变状态,有助于对患者及其家系进行遗传风险管理,包括家系验证、制定筛查方案、化学预防、预防性手术、生殖干预等。
2)HRR基因突变
HRR是一个复杂的生物学过程,开始于细胞内DNA损伤感应蛋白质对于DSB的识别,这个过程主要依赖于MRN(MRE11、RAD50、NBS1)蛋白复合物,随后在DNA酶的作用下由5’到3’对DNA进行切割,ATM、RPA等蛋白结合于突出的单链DNA阻止其进一步降解;以RAD51为核心的DNA重组酶随后结合于单链DNA并在姐妹染色单体上寻找同源序列以作为后续DNA修复的模板,在这个过程中,RAD51借由BRCA2募集到RPA结合的单链DNA上,而BRCA2的募集则依赖于BRCA1和PALB2。
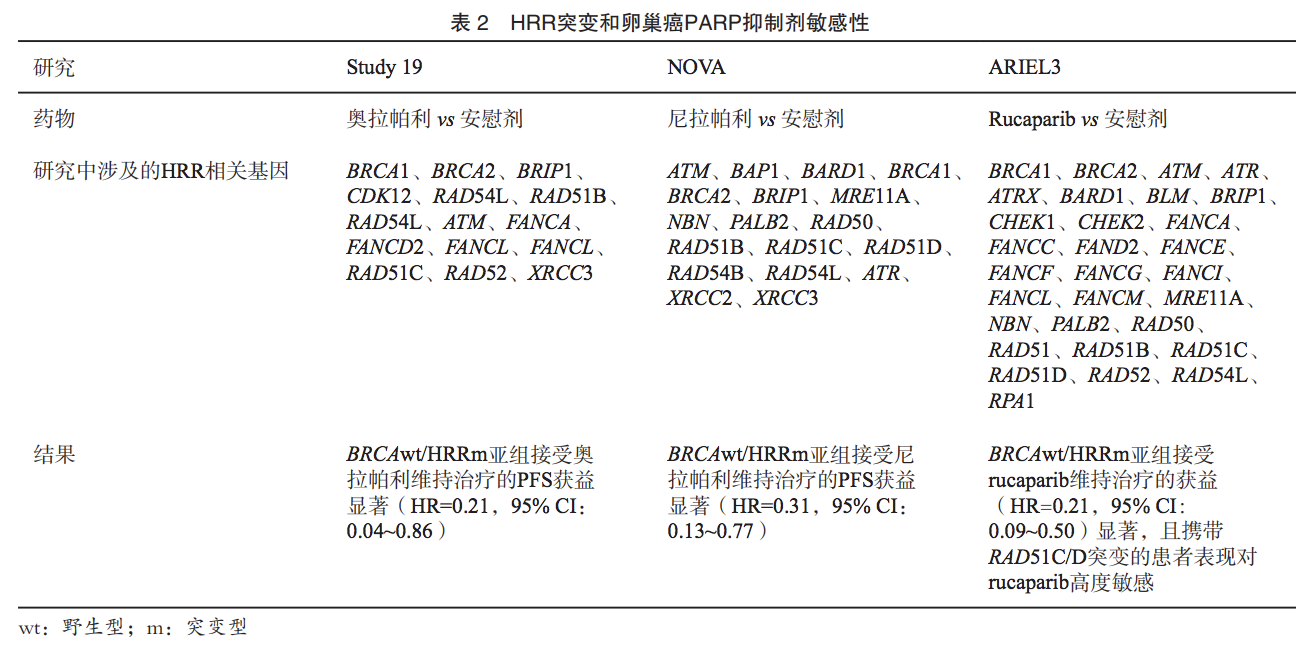
3)BRCA1/RAD51C启动子甲基化
基因的表观遗传学变化同样可能引起细胞发生HRD,卵巢癌中较常见的是BRCA1和RAD51C的启动子甲基化,BRCA1或RAD51C的甲基化将导致对应的基因表达下调,并且通常与BRCA1/2或其他HRR相关基因的变异互斥。
在患者来源异种移植瘤(patient-derived xenograft,PDX)小鼠模型、卵巢癌细胞系及PARP抑制剂的临床研究中发现,BRCA1或RAD51C甲基化与rucaparib的敏感性相关,纯合BRCA1甲基化对rucaparib高度敏感,而杂合BRCA1甲基化对rucaparib表现出耐药。
4)HRD状态
在新诊断的卵巢癌中,BRCA1/2和HRD检测被推荐用于指导一线卵巢癌的治疗方案选择。除此之外,包括突变特征Signature 3、HRDetect、功能性HRD检测(RAD51 Foci)等在内的新兴生物标志物及检测方法对于PARP抑制剂敏感性的预测也在研究之中。
PARP抑制剂生物标志物检测建议
基于国内外指南及共识的推荐、PARP抑制剂国内外药物适应证,以及中国卵巢癌患者临床诊疗现状,经过专家组讨论,对中国卵巢癌患者PARP抑制剂相关的生物标志物检测进行如下推荐:
1)推荐所有非黏液性卵巢癌患者在初次病理学检查确诊时,明确肿瘤BRCA1/2的突变(包括胚系和体细胞突变)状态,对于Ⅰ期患者仅需明确胚系BRCA1/2突变状态(1类)。具体如下:
①如果患者仅行肿瘤组织BRCA1/2检测,且突变状态为阳性,建议进一步采用血液或唾液样本进行BRCA1/2胚系检测,以明确该变异是否为胚系变异(1类)。②如果患者仅行肿瘤组织BRCA1/2检测,且突变状态为阴性,建议进一步对血液样本进行大片段重排(large genomic rearrangement,LGR)变异的检测以明确是否存在BRCA1/2的胚系LGR变异(1类)。③如患者仅行胚系BRCA1/2检测,且结果为阳性,则无需再对肿瘤组织进行BRCA1/2检测(1类)。④如患者仅行胚系BRCA1/2检测(包含针对LGR的MLPA检测),且结果为阴性,则需要对肿瘤组织进行BRCA1/2检测(1类)。⑤根据当地检测策略并综合成本效益,可以同时进行BRCA1/2的胚系及肿瘤突变检测,或胚系、肿瘤检测序贯进行(2A类)。
2)对于新诊断的晚期卵巢癌患者(目前主要证据在高级别浆液性卵巢癌和高级别子宫内膜样癌),HRD状态(包括BRCA1/2和HRD score)有助于医师选择不同维持治疗方案以期达到最佳治疗效果:
①建议进行HRD检测(包括BRCA1/2和HRD score)(2A类);如患者存在抗血管生成抑制剂治疗的禁忌证,或不考虑抗血管生成抑制剂治疗时,HRD状态对于维持治疗的疗效预测及预后判断仍有参考价值(2B类)。②如既往接受过肿瘤BRCA1/2检测,且结果为阳性,不需要再补充进行HRD检测(1类)。③如既往接受过肿瘤BRCA1/2检测,且结果为阴性,建议对肿瘤样本进行HRD检测以明确是否为HRD阳性(2A类)。④当HRD检测不可及时,可考虑对肿瘤组织进行HRR基因检测(3类)。
3)对于铂敏感复发的卵巢癌患者,BRCA1/2突变状态及HRD状态并不作为含铂类药物化疗后PARP抑制剂维持治疗的选择标准,但对于患者疗效预测及预后判断具有一定的参考价值:
①既往已经接受过BRCA1/2或HRD的检测,即便有更新的肿瘤样本可及时,也暂不推荐对同一检测项目重复进行检测(2A类)。②可考虑进行HRD检测(包括BRCA1/2和HRD score)(2B类)。③如既往接受过肿瘤BRCA1/2检测,且结果为阳性,不需要补充HRD检测(1类)。④如既往接受过肿瘤BRCA1/2检测,且结果为阴性,可考虑进行HRD检测(2B类)。⑤当HRD检测不可及时,可考虑进行肿瘤组织HRR基因检测(3类)。
4)对于考虑使用PARP抑制剂作为单药挽救性治疗的后线卵巢癌患者:
①既往已经接受过BRCA1/2或HRD的检测,即便有更新的肿瘤样本可及时,也暂不推荐对同一检测项目重复进行检测(2B类)。②铂敏感复发的患者,推荐进行HRD检测(包括BRCA1/2和HRD score)(2A类)。③铂耐药复发的患者,仅需接受胚系和(或)肿瘤BRCA1/2检测(2A类)。④当HRD检测不可及时,可考虑进行肿瘤组织HRR基因检测(3类)。
参考来源:
中国抗癌协会妇科肿瘤专业委员会,中华医学会病理学分会.上皮性卵巢癌PARP抑制剂相关生物标志物检测的中国专家共识.《中国癌症杂志》2020年第30卷第10期.






